再発・転移性膀胱がんの治療に新薬登場! 尿路変向の選択や、膀胱全摘前後の補助化学療法の長所・短所などの十分な理解が大切

2018.5 取材・文:町口 充
膀胱がんの治療に関する最新情報は、「膀胱がんを知る」をご参照ください。
膀胱がんは、肉眼で確認できる血尿や痛みなどの症状が出て診断されることが多く、約70~75%の患者さんはがんが粘膜あるいは粘膜下に留まる筋層非浸潤性膀胱がんとして発見されます。がんが進行し、筋層まで達する筋層浸潤性膀胱がんは約20~25%の膀胱がんで認められますが、その標準治療は膀胱全摘です。限定されたケースでは膀胱温存療法も選択肢の1つとなります。他臓器への遠隔転移などがあればステージIVとなり、治療選択は全身化学療法がメインとなります。全身化学療法に治療抵抗性を示したがんに対する2次治療はこれまでに存在しませんでした。しかし2017年12月から新たな治療法である免疫チェックポイント阻害薬が登場しました。
遠隔転移のない筋層浸潤性膀胱がんの標準治療は膀胱全摘+リンパ節郭清
膀胱の一番内側を覆う尿路上皮(粘膜上皮)から生じたがんが粘膜下層を越えて筋層にまで浸潤したがんが筋層浸潤性膀胱がんです。粘膜に留まっている筋層非浸潤性膀胱がんであれば内視鏡による切除 (経尿道的膀胱腫瘍切除術:TURBT)でがんを切除できますが、筋層にまで達した筋層浸潤性膀胱がんのケースでは一般的に、膀胱全摘が選択されます。
筋層にまで浸潤した膀胱がんでは、内視鏡による切除のみではがんが膀胱壁を貫いて隣接する器官に浸潤したり、リンパ節や肺、肝臓、骨などに転移する危険性が高まります。膀胱全摘をした場合と、全摘をしないで全身化学療法や放射線療法を行った場合、あるいは無治療で経過観察を行った場合と比較すると、膀胱全摘を施行することで最も高い生存率が得られることがわかっています。
膀胱全摘では、膀胱以外の臓器も摘出します。男性では膀胱、前立腺、精嚢をまとめて摘出します。女性では膀胱、子宮、腟の一部をまとめて摘出しますが、がんの大きさによっては子宮や腟を残す場合もあります。男女とも、このほかに膀胱につながる尿管の一部と、尿道再発のリスクが高いと予想される場合には尿道の摘出も行われます。
また、膀胱全摘を行う際は、膀胱に隣接した骨盤内のリンパ節を取り除くリンパ節郭清も行われます。リンパ節に転移しているかどうかは手術前にCT検査などで確認します。リンパ節転移があったケースは予後が悪いことがわかっています。そのため、手術後に化学療法を追加して行う必要があるかどうかなどの治療方針を決めるうえでも、リンパ節を採取して病理所見を確認することは重要です。また、膀胱がんはリンパ節郭清を行うことで予後が改善するとの研究報告があり、治療効果の面でもメリットがあります。
膀胱全摘の際、選択される3つの尿路変向、尿管皮膚、回腸導管、回腸利用新膀胱
膀胱を全摘すると腎臓でつくられた尿を体外に排出する尿路がなくなるため、尿路変向(変更)と呼ばれる再建手術が必要となります。いくつかの方法がありますが、大別すると非禁制型(尿失禁型)と禁制型に分けられます。「禁制」とは「尿漏れを防ぐ」という意味で使われます。(表1参照)。
非禁制型の代表的術式には尿管皮膚瘻と回腸(結腸)導管があります。 尿管皮膚瘻は切断した左右の尿管を直接皮膚の外に出し、そこから尿を出す方法です(図1参照)。
回腸導管は回腸の一部を遊離し、それに尿管をつないだうえで導管先端を皮膚の外に出し、尿の出口にする方法です(図2参照)。いずれも尿をためる(蓄尿)機能を有しておらず、断続的に流れてくる尿をためる収尿袋 (装具)をつける必要があり、収尿袋に尿がたまったら適宜トイレに流します。
蓄尿機能を有するタイプである禁制型尿路変向の代表は回腸利用新膀胱です。回腸の一部を遊離して尿をためる袋(新膀胱)を腹腔内につくり、この袋に尿管と尿道をつなぐ方法です(図3参照)。尿道から尿が出せるのでトイレに行って腹圧による自力での排尿が可能(自排尿型尿路変向)です。
禁制型尿路変向には、この自排尿型尿路変向のほかに、自己導尿型尿路変向があります。自己導尿型尿路変向は腸の一部を遊離して尿をためる袋 (パウチ)を腹腔内につくりますが、これを皮膚につなげます。定期的に皮膚の出口からパウチに自分で細いカテーテルを入れて尿を排出する処置が必要となります。この手術は手術時間も長く、合併症も多いため、近年ではあまり実施されていません。
表1 尿路変向の種類と特徴
| 尿管皮膚瘻 | 回腸導管 | 回腸利用新膀胱 |
| 排尿方法 | ||
| 非禁制型(尿失禁型) | 禁制型 | |
| 排尿はできない | 排尿はできない | 尿道から排尿が可能 |
| ストーマに装着した収尿袋(装具)に継続的に尿がたまる。収尿袋に溜たまった尿を適宜トイレに流す | 尿意は生じないため、下腹部の張りを感じるなど尿のたまったタイミングで、お腹に力を入れて排尿 | |
| 条件・特徴 | ||
| 収尿袋の管理ができること、尿路のストーマができることに対する理解が得られていること | 尿漏れすることがあるので、尿パッドが必要となることがある | |
| 比較的短時間の手術で作成できる | 患者さんの手術適応の範囲は広い | 尿道にがんが及んでいる、または、尿道再発の恐れが高い場合には適応外 |
| 回腸利用にリスクのある場合に選択される | 回腸利用にリスクのある場合(クローン病などの腸疾患)は実施できない | |
| 尿管にステントが留置される場合は定期的な交換が必要 | 術前より腹圧性尿失禁のある場合は適応外 | |
| 腎盂腎炎が起きやすい | 尿が十分出し切れない場合は、自分で尿道から細いカテーテルを入れて尿を排出する処置(自己導尿)が必要となる | |
| 術後しばらくの間は新膀胱 (代用膀胱)が腸粘液で詰まることがあり、適宜尿道からカテーテルを入れて代用膀胱を洗浄する必要がある | ||
図1 尿管皮膚瘻の完成図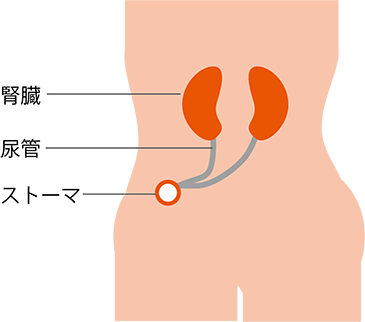
図2 回腸導管の完成図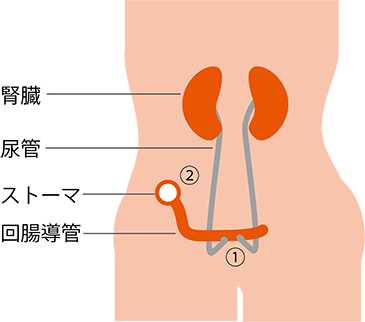
(1)15~20cmほど切り離した回腸に尿管をつなぐ
(2)回腸の端を皮膚の外に出して、ストーマ孔にする
図3 回腸利用新膀胱造設術の流れ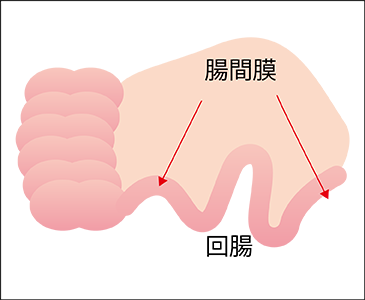
回腸を40~60cmほど切り離す
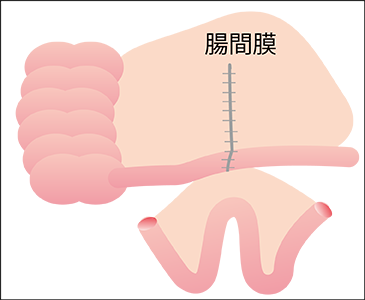
食事の通り道の確保のため回腸どうしをつなぎ合わせる
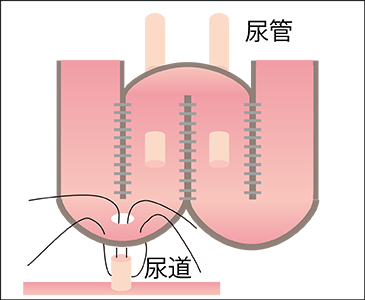
遊離した回腸を切開し、1枚のシート状にして尿管と尿道をつなぐ
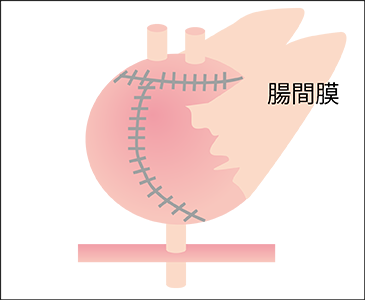
回腸で作成したシートを球状に縫合して新膀胱をつくる
回腸導管は適用範囲が広く一般的、尿道に再発リスクがなければ自排尿型を選ぶ場合も
これらのうち、尿管皮膚瘻は手術の方法が単純なため短時間で作成でき、患者さんの体の負担が一番少ない方法です。しかし、腎盂腎炎などの細菌感染が起きやすく、また尿管からの尿の排出をスムーズにするため、しばしば尿管にステントという人工の管を入れておく必要があります。このステントは定期的に交換が必要となります。合併症を有している高齢者や、腸に疾患があるなどで腸管が利用できない場合などに選択される術式です。
回腸導管は古くから行われている手術で、適応範囲が広く、膀胱全摘が可能なほぼすべての患者さんで選択される術式です。
尿道に疾患や再発のリスクがない患者さんでは、自排尿型尿路変向である回腸利用新膀胱造設術が選択できます。
治療効果を高めるために膀胱全摘の前に術前補助化学療法を行う
筋層浸潤性膀胱がんの標準治療は膀胱全摘ですが、手術だけの治療での5年生存率は50%程度といわれており、治療成績向上のために術前あるいは術後の補助化学療法が必要とされています。
大規模な臨床試験からシスプラチンを含む多剤併用の術前補助化学療法は生存率を高める効果があることがわかっています。また術前補助化学療法は、目に見えない微小転移に対して、より早期に対応することができるなどの利点があります。これに対して術後補助化学療法は、手術で摘出した原発巣の病理診断をもとにして治療が必要な患者さんをより的確に選ぶことができるなどの利点があります。
一方、術前補助化学療法を行う場合は、膀胱全摘の手術時期が遅れることに患者さんが不安をもつことも少なくありません。がんの進行により血尿が強かったり、尿の通過が障害され腎臓が腫れ(水腎症)、腎機能が低下している患者さんに対しては膀胱全摘を先行させることが望ましい場合もあり、実際に術前補助化学療法を実施する患者さんの割合は3割程度にとどまります。
術前補助化学療法の投与のタイミングや、薬の組み合わせ、投与量、スケジュール、コース数などについては議論があり、定まっていません。当院では、ゲムシタビン(製品名:ジェムザール)+シスプラチンの2剤を組み合わせたGC療法を、21日周期で3コースから4コース行っています。
深達度T3aなどの条件を満たせば、膀胱温存という選択肢
筋層浸潤性膀胱がんの標準治療は膀胱全摘であるのに対して、近年、いくつかの施設で、膀胱を全摘せずに治療する膀胱温存療法を行って良好な成績を示せたという報告が相次いでおり、なかには、放射線を使って膀胱温存療法を行ったところ5年生存率が膀胱全摘に匹敵するような成績だったという報告もあります。このため、日本泌尿器科学会が作成した診療ガイドラインでも、「標準治療外であることを了承したうえで膀胱温存を希望する症例が対象」とし、深達度T3a(筋層を越えて脂肪組織への顕微鏡でわかる浸潤がある)以下の限局がん、腫瘍径が3cm以下であること、上皮内がん(CIS)という平坦型のがんを伴わないこと、かつ水腎症のない症例に限定して膀胱温存療法を選択すべきとしています。膀胱温存治療は放射線照射単独だけでは不十分です。ガイドラインでは、積極的に膀胱温存を図る場合には内視鏡による経尿道的膀胱腫瘍切除術(TURBT)でできる限りがんを取り除いたうえで、シスプラチンを中心とした化学療法、および放射線療法を併用することを推奨しています。
遠隔転移がある場合、または膀胱全摘後がんが再発した場合は、全身化学療法を行う
遠隔転移を有する膀胱がん、あるいは膀胱全摘後にがんが再発した場合、治療法として選択されるのは全身化学療法で、最初に行う1次治療は、ゲムシタビン+シスプラチンのGC療法です。GC療法が登場する前には、メトトレキサート(製品名:メソトレキセート)+ビンブラスチン(製品名:エクザール)+ドキソルビシン(製品名:アドリアシン)+シスプラチンの4剤を組み合わせたMVAC療法が行われていました。しかし、GC療法とMVAC療法を比較した臨床試験で治療効果は同等であるもののGC療法で重篤な副作用が少ないことがわかり、現在、1次治療として推奨されているのはGC療法です。
海外では、投与期間を短縮させてより高い効果を狙うdd(dose dence:ドーズデンス)MVAC療法により生存率を有意に改善させたとの報告があり、NCCN(全米総合がん情報ネットワーク)のガイドラインでは1次治療の1つとなっています。また、欧州のガイドラインでは、ddMVAC療法に加え、ゲムシタビン+シスプラチン+パクリタキセル(製品名:タキソール)の3剤併用によるPCG療法も1次治療に加えられています。
日本の診療ガイドラインで推奨されている転移性膀胱がんの1次治療はGC療法とMVAC療法のみですが、臨床試験などで有用性が認められれば、ddMVAC療法やPCG療法も選択肢となるかもしれません。
転移性膀胱がんの2次治療として登場した免疫チェックポイント阻害剤
GC療法が効かなくなったとき、転移性あるいは再発性膀胱がんに対する2次治療については、これまで有効性を示す治療法がなく、患者さんの全身状態に合わせてさまざまな治療法を順次試していく状況でした。そこへ2017年12月、免疫チェックポイント阻害薬であるペムブロリズマブ(製品名:キイトルーダ)が進行性尿路上皮がんの2次治療として日本で承認されました。尿路上皮がんとは、尿路(腎盂、尿管、膀胱、尿道)に発生するがんのことで、大部分が膀胱がんです。
この治療薬の効く仕組みは、これまでの抗がん剤と大きく異なっています。免疫にかかわるT細胞は、異物を見つけると攻撃しますが、過剰に働かないように制御する機能も備わっています。そのブレーキの働きを担うのが免疫チェックポイントです。がん細胞は、この免疫チェックポイントに巧みに信号を送り、免疫にブレーキをかけさせてT細胞の攻撃から逃れています。ブレーキをかける信号は、T細胞表面のPD-1という物質に、がん細胞表面にあるPD-L1が結合することによって発信されます。ペムブロリズマブは抗PD-1抗体と呼ばれる薬で、PD-L1より先にT細胞のPD-1に結合することによりがん細胞からの信号を遮断してしまいます。この結果、抑制されていたT細胞が再び活性化され、抗がん作用が発揮される仕組みです。
1次化学療法が効かなくなった患者さんに対する試験(KEYNOTE-045試験)の結果では、2次治療として従来使用してきたパクリタキセルなどの化学療法とペムブロリズマブ単剤療法とを比較したところ、全奏効率では前者の11.0%に対して21.1%、全生存期間(中央値)は7.3か月に対して10.3か月と有意に延長し、ペムブロリズマブの有効性が確認されました。副作用の内容も大きく異なり、抗がん剤はさまざまな副作用が出ますが、ペムブロリズマブの副作用はそう痒感、疲労、吐き気といった症状が10%程度みられるものの、グレード3以上の重篤な副作用の発現率が5%を超えるものはありませんでした。新しい薬の登場は患者さんにとっての希望の光となるものです。今後の免疫チェックポイント阻害薬を中心とした新たな2次、3次治療の開発に注目が集まっています。
膀胱がんの確定しているリスク要因は喫煙です。禁煙など予防を心がけ、定期的に検査を受け、少しでも症状があれば医療機関を受診して診てもらうことで、より早期に治療を開始することができます。
プロフィール
菊地栄次(きくち・えいじ)
1994年 慶應義塾大学医学部泌尿器科入局
2001年 米国メモリアルスロンケタリングがんセンター留学
2009年 慶應義塾大学医学部泌尿器科専任講師
2017年 慶應義塾大学医学部泌尿器科准教授

