悪性胸膜中皮腫、がんウイルス療法の臨床試験を開始
2018/08/16
文:がん+編集部
悪性胸膜中皮腫に対するがんウイルス療法の臨床試験が、2018年9月頃から開始されます。再発した腫瘍に対しては有効な治療法がない悪性胸膜中皮腫の新たな治療法として、期待されます。
手術適応のない再発または進行性の悪性胸膜中皮腫患者さんが対象
東京大学医科学研究所附属病院は8月2日、悪性胸膜中皮腫に対するがんウイルス療法の臨床試験を2018年9月頃から開始すると発表しました。
悪性胸膜中皮腫は、主に胸腔に発生するがんで、アスベスト(石綿)が主な原因と考えられています。初期の段階では、自覚症状があまりなく、進行すると胸水がたまり、胸痛、息切れ、咳嗽(がいそう)、体重減少などの症状が現れます。治療は手術、放射線治療、化学療法が行われますが、とくに再発した腫瘍に対しては、現在、有効な治療法がありません。
がんウイルス療法とは、がん細胞のみで増えることができるウイルスを感染させ、ウイルスが直接がん細胞を破壊する治療法です。がんウイルス療法では、がん細胞では増えても正常細胞では全く増えないウイルスを人工的につくって使用します。がん細胞のみで増えるようにつくられたウイルスは、がん細胞に感染するとすぐに増殖を開始し、感染したがん細胞を死滅させます。増殖したウイルスはさらに周囲に散らばって他のがん細胞に感染し、次々にがん細胞を破壊していきます。一方、正常細胞ではウイルスが増えないようにつくられているため、正常組織は傷つけません。最近では、米アムジェン社が開発を進める、単純ヘルペスウイルス1型(talimogene laherparepvec)が悪性黒色腫の治療薬として欧米で承認されています。
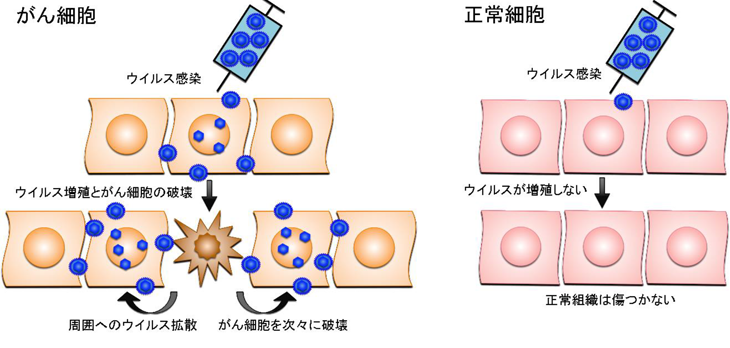
画像はリリースより
今回の臨床試験で使用される、治療用単純ヘルペスウイルス1型のG47Δ(ジーよんじゅうななデルタ)は、膠芽腫(悪性脳腫瘍)患者さんを対象に、第2相臨床試験がおこなわれています。また、前立腺がんや嗅神経芽細胞腫患者さんを対象とした臨床試験も実施されました。また、G47Δは、厚生労働省の先駆け審査指定制度※1の対象品目に指定され、悪性神経膠腫に対する希少疾病用再生医療等製品※2に指定されています。
今回の臨床試験の概要は、以下の通りです。
対象疾患:手術適応のない再発または進行性の悪性胸膜中皮腫
投与方法:胸腔内への投与。胸腔内投与ができなくなるまで、もしくは腫瘍が治療に反応せず進行するまで、4週間毎に繰り返し投与(最大6回)。
予定症例数:6例
目的:安全性と治療効果の評価
評価期間:最終投与後3か月間
試験開始時期:2018年9月頃
※1 革新的医薬品や医療機器・体外診断用医薬品・再生医療等製品について、世界に先駆けて日本での早期実用化を目指す厚生労働省の施策の1つです。生命に重大な影響がある重篤な疾患等に対して、極めて高い有効性が期待される医薬品や再生医療等製品等を指定し、日本の患者さんに世界で最先端の治療薬を最も早く提供することを目指しています。
※2 医療上の必要性が高いにもかかわらず、患者数が少ないために治療法の開発が十分に進まない状況に対応し、安全かつ良質な再生医療等製品を一日も早く医療の現場に提供するための制度です。指定されると、優先審査や再審査期間の延長などの支援措置が受けられます。

