がんゲノム医療―遺伝子情報に基づくプレシジョン・メディシン(精密医療)とは

ゲノム生物学研究分野 分野長河野隆志先生
2021.12 取材・文:がん+編集部
がんは、遺伝子変異が原因で起こる病気です。遺伝子に変異が起こることで異常なタンパク質が作られ、がん細胞となります。変異した遺伝子が作り出す異常なタンパク質をターゲットにした分子標的薬が開発され、遺伝子情報に基づくがんゲノム医療が推進されています。そこでは、コンパニオン診断や遺伝子パネル検査が重要な役割を果たしています。ここでは、がんと遺伝子の関係、がんゲノム医療の現状と未来に関して解説します。
がんと遺伝子の関係―ほとんどのがんは遺伝子の変化で起こる病気
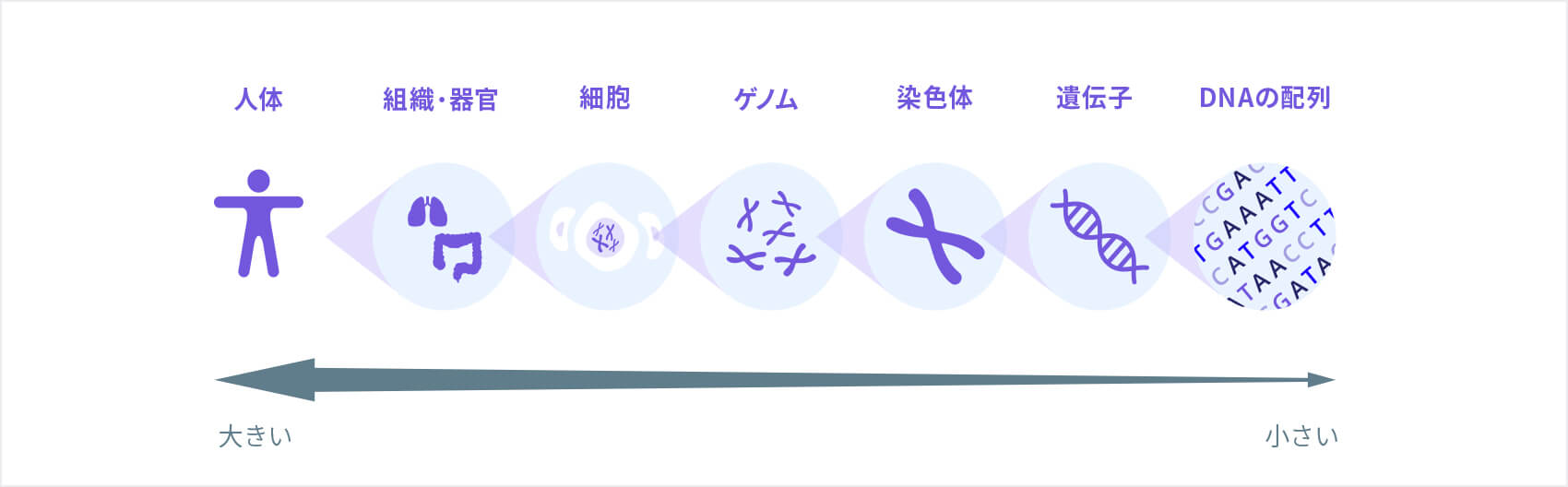
ヒトの体は数十兆個の細胞からできています。1つ1つの細胞は、遺伝子によってコントロールされ、遺伝子に記された設計図となる情報に基づき、適切なタイミングで適切な量のタンパク質が作られます。しかし、ある遺伝子に何らかの変化が生じて正しく働かなくなることで、細胞が正常に機能しなる場合があります。正しく働かなくなった細胞が無秩序に増殖するようになると、そこからがんが発症することがあります。
遺伝子に変化が起こる原因は
正常に機能できなくなるような変化が遺伝子に起こる原因として、加齢、喫煙、食生活、紫外線など、生活習慣や環境要因によるものがあるとわかっています。こうした原因により遺伝子が変化しても、体の細胞にはそうした遺伝子を元通りに修復する仕組みがあるため、1つだけ起きた変化によってすぐに細胞ががん化するわけではありません。
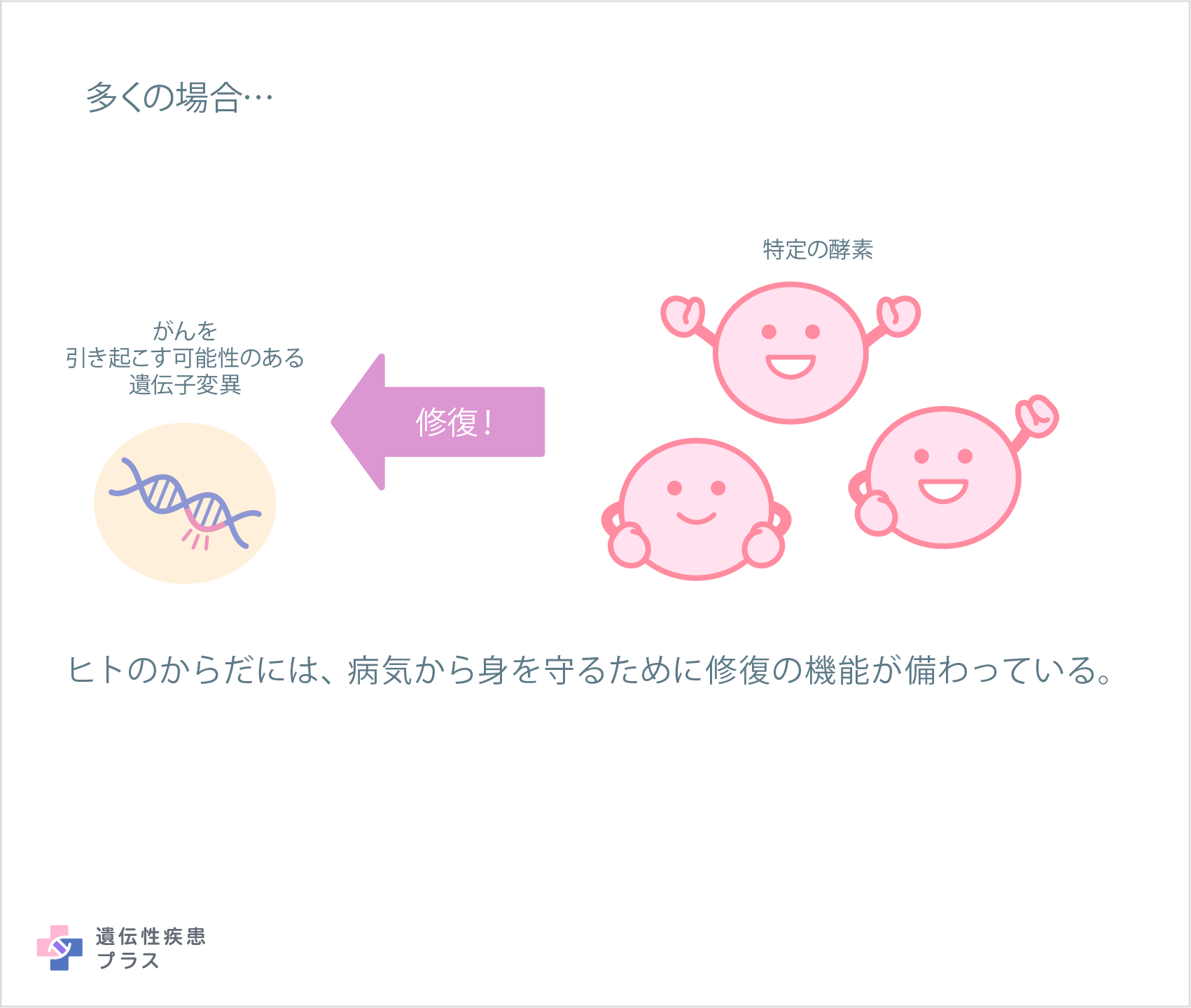
出典:遺伝性疾患プラス「遺伝子変異と健康 すべての遺伝子変異は健康と発達に影響を及ぼしますか?」イラストをもとに許可を得て一部改変
遺伝子の変化(変異・融合遺伝子)とは
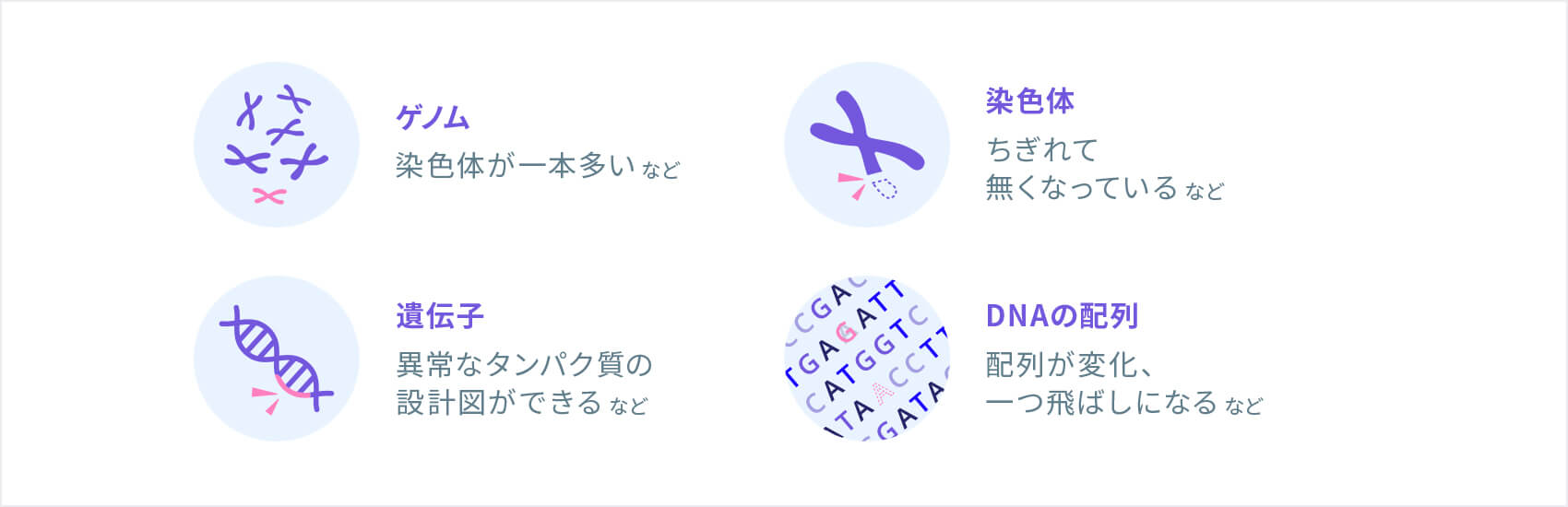
遺伝子はDNAという物質でできています。DNAは、「アデニン(A)」「チミン(T)」「グアニン(G)」「シトシン(C)」の4種類の「塩基」と呼ばれる物質で構成されています。前述のように生活習慣や環境要因など、何らかの原因によって、4つの塩基のどれかが別の塩基に置き換わったり、一部の塩基が単独または連続で欠けたり、あるいは、そこになかった塩基が付け加えられたりすることがあります。こうした変化を「遺伝子変異」といい、遺伝子変異によって、遺伝子に記された設計図の情報が書き換えられてしまうことがあります。
また、遺伝子が途中でちぎれ、別の遺伝子と結合して1つの遺伝子のようになってしまうことがあります。こうしたできた遺伝子を「融合遺伝子」といいます。例えば非小細胞肺がんの原因遺伝子の1つである「ALK融合遺伝子」や、慢性骨髄性白血病の原因遺伝子の1つである「BCR-ABL」も、「融合遺伝子」です。
遺伝性のがんとの違い
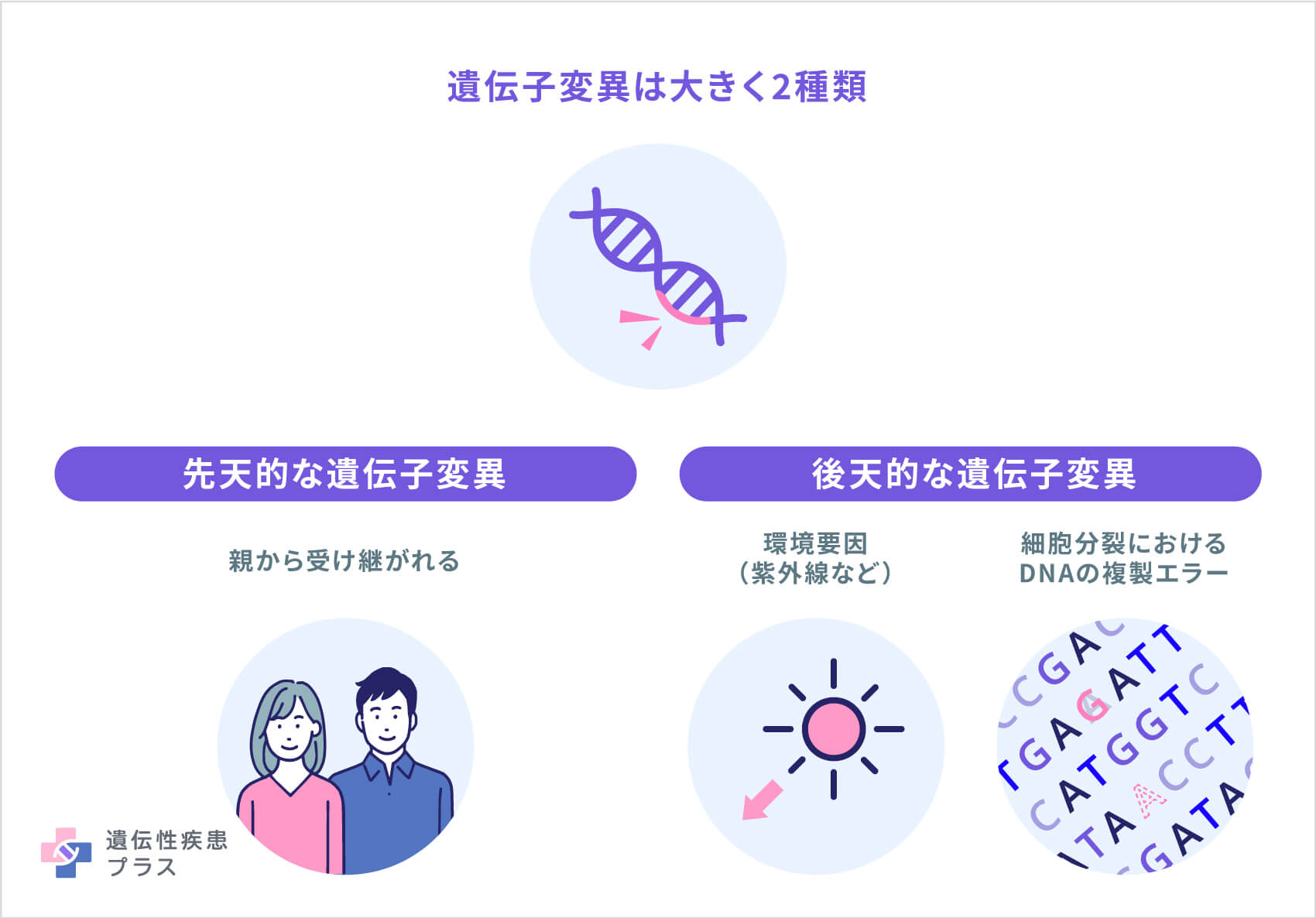
生活習慣や環境要因などによる遺伝子の変化を原因とするがんは、基本的に次の世代(子ども)に遺伝することはありません。しかし、生まれ持った遺伝子の違いにより、一部のがんになりやすい体質の人がいます。このような、「がんになりやすいタイプの遺伝子が原因」で発症するがんを「遺伝性腫瘍」といいます。がんになりやすいタイプの遺伝子を持っていても、全員が必ずがんになるとは限りません。
がん遺伝子検査とは
がんの保険診療では、治療法の決定のために特定の染色体や遺伝子に変異があるかの検査が行われます。保険診療として行われるがんの遺伝子の検査の主なものとして、「コンパニオン診断」と「がん遺伝子パネル検査」があります。
コンパニオン診断
コンパニオン診断は、特定の治療薬の効果や副作用を治療前に予測するための遺伝子検査です。一部のがん種では、特定の遺伝子変異が原因の場合に効果が得られる治療薬が開発されています。非小細胞肺がんでは、「EGFR遺伝子変異」「ALK融合遺伝子」「ROS1融合遺伝子」「BRAF遺伝子変異」「MET遺伝子変異」「RET融合遺伝子」に対する治療薬が承認されており、これらの遺伝子変異に適した薬剤による治療が推奨されています。
がん遺伝子パネル検査
がん遺伝子パネル検査は、がん細胞に起きている遺伝子の変化を全体的に調べ、がんの特徴を知るための検査です。多くの遺伝子を一度に調べることができますが、コンパニオン診断とは異なり、必ずしも治療に直結した情報が得られるというものではありません。遺伝子に変異が見つかっても、その変異に適した薬剤がない場合などもあり得ます。2019年10月末時点の厚生労働省の調査によると、がん遺伝子パネル検査を受け、遺伝子の変異に結び付いた治療薬の投与がなされた患者さんの割合は10.9%でした。
がん遺伝子パネル検査は、「保険診療で受けられもの」「自由診療となるもの」「研究として行われるもの」があります。保険診療での検査の対象となるのは、標準治療がない固形がん、局所進行または転移があり標準治療が終了した(終了見込みを含む)固形がんの患者さんです。
がん遺伝子パネル検査の必要性
近年、がん遺伝子の研究が進み、遺伝子の特性に適した治療薬の開発が進んでいます。また、がんが発生した部位(がん種)ごとではなく、「固形がんが対象」というように同じ遺伝子の特性をもつ複数のがん種に対しての臨床試験も行われ、一部の治療薬では複数のがん種を対象に承認されている治療薬も登場しています。
がん遺伝子パネル検査で遺伝子変異が見つかり、その遺伝子変異に対する治療薬が存在しても、まだそのがん種に対しては承認されていない、といったケースもあります。しかし、がん種を超えて遺伝子の特性に適した治療薬としての臨床試験が行われていれば、臨床試験に参加することで治療を受けることもできます。
また、患者さんの数が少ない希少がんなどでは、がん種ごとに臨床試験を行うことが難しく、治療法を開発し難いという現状があります。しかし、がん種ではなく遺伝子ごとであれば、ある程度の人数の患者さんを集めることができ、臨床試験を行うことができます。こうしていくことにより、新たな治療法の開発にもつながっていきます。
がん遺伝子パネル検査は、がんの特性を見つけることで、適した治療法を提供するだけでなく、新たな治療開発や研究の基盤となるデータを蓄積するためにも必要とされています。
遺伝子の変化を標的にしたがん治療とは
遺伝子の変異を標的とした治療薬は、遺伝子そのものを治すわけではありません。変異した遺伝子から作り出される異常なタンパク質を標的として、そのタンパク質の機能を抑えます。
例えば、非小細胞肺がんの約半数の患者さんでは、上皮成長因子受容体(EGFR)を作り出すEGFR遺伝子に変異が認められます。EGFR遺伝子に変異が起こると、その遺伝子から作られるEGFRというタンパク質が正常に機能できなくなります。具体的には、上皮細胞の増殖を促すシグナル伝達に関わる「チロシンキナーゼ」という酵素活性をEGFRは持っているのですが、変異によりこれが常に活性化され、がん細胞が増殖を繰り返します。EGFR遺伝子変異がある非小細胞肺がんの患者さんに対する治療薬として使われる「EGFRチロシンキナーゼ阻害薬」という薬剤は、増殖シグナルを出し続ける「チロシンキナーゼ」という酵素の機能を阻害することでがんの増殖を抑制します。
こうした薬剤は、変異遺伝子が作り出す異常なタンパク質を標的にして、その異常な働きを抑えます。このようにタンパク質など特定の分子を標的とした薬剤を「分子標的薬」といいます。
がんゲノム医療の未来
がんゲノム医療は、がん細胞のゲノムを調べ、1人1人の患者さんのがんの遺伝子にどのような変化が起こっているのかを知ることで、がんの特性に合わせた治療選択をする医療です。そのために必要なのが遺伝子検査です。
がんの外科手術は、がん種ごとに行われています。がんの薬物治療も、これまで、がん種ごとに承認された抗がん剤による治療が中心に行われてきました。しかし、最近では分子標的薬の登場により、がん種ではなく、遺伝子の変異に合わせた治療が行われるようになってきています。また、分子標的薬の効果を事前に調べるコンパニオン診断が導入されたことで、効果が期待できる患者さんを予測できるようになりました。さらに、2019年にがん遺伝子パネル検査が承認されたことで、一度に多くの遺伝子変異を調べ、がんの特性を総合的に判断して最適な治療を検討することも可能になりました。
がんの原因となる遺伝子変異の研究や検査技術の進歩により、がん患者さん1人1人に合わせた治療を行うプレシジョン・メディシン(精密医療)が実用化に向けて着実に進んできています。
C-CATが担うがんゲノム医療
国のがん対策の1つとして、がんゲノム医療を支援するために、「C-CAT(Center for Cancer Genomics and Advanced Therapeutics)」というがんゲノム医療に関連する情報を集めて管理する機関が設立されました。C-CATでは、がん患者さんの治療支援はもちろん、がんゲノム情報に基づく医療の発展や向上のためにさまざまな取り組みが行われています。
C-CATの主な役割は、3つです。
- 患者さん1人1人のがんのゲノム解析の結果得られる情報および診療情報を集約・保管したデータベースを管理・運営すること
- がんゲノム医療を行う病院とデータを共有し、がんゲノム医療の質の確保・向上に役立てること
- 大学などの研究機関や製薬会社などの企業で行われる研究開発のための基盤を提供すること
がん遺伝子パネル検査を受けたときに、検査結果や診療情報をC-CATに提供すると、その患者さんに適した治療選択に役立つ情報、例えば、同じ遺伝子変異をもっている別の患者さんに効果があった薬剤や副作用の情報を担当医は知ることができます。そしてこの担当医を介して患者さんはより効果の高い治療を受けることができます。つまり、自身のゲノム情報をC-CATに提供した患者さんに、治療情報として還元されるという仕組みです。
C-CATデータの利活用―C-CAT利活用検索ポータル
C-CATでは、2.5万人以上の患者さんのデータを基にした医療の発展と向上を目的とした「C-CAT利活用検索ポータル」というサービスを2021年10月に開始しました。毎年1万8,000人程度の患者さんの情報が追加されていくため、数年以内に10万人規模のデータが集まる予定です。この検索サイトを使えば、日本人では「どのがん種」で「どのような遺伝子変異が多くあるのか」などがわかるようになります。100人程度のデータではわからなかったものが、数千人という規模になれば見えてくる可能性があります。
また、治療薬と遺伝子変異を組み合わせて検索することも可能です。例えば、免疫チェックポイント阻害薬による治療効果があった患者さんで多く認められた遺伝子変異がどのようなものがあったのか、といったこともわかります。治療法と遺伝子変異の関係がわかることで、同じ遺伝子変異を持つ別の患者さんに対し、免疫チェックポイント阻害薬の効果予測として活用できる可能性があります。
さらに、がん種による遺伝子の新たな特徴や、新たな治療標的が見つかる可能性もあり、研究や治療薬の開発の種となるような活用法も期待されます。
C-CATデータの利活用―診療検索ポータル
C-CATでは併せて「診療検索ポータル」という診療支援を目的としたサービスを全国220以上の病院に提供しています。このサービスはがんゲノム医療病院向けのもので「臨床試験のアップデート」という機能がついています。担当医が受け持つ患者さんを検索すると、実施中の臨床試験が表示されるため、患者さんの適格条件にあった臨床試験を見つけることができます。
C-CATに蓄積されたデータの一部は、厳格な審査ののち、医療機関、大学や製薬企業などの研究機関に「利活用検索ポータル」を通じて提供されはじめており、新たな治療薬の研究開発に用いられています。ここで生まれた成果は将来のがん患者さんのために役立てられます。がん遺伝子パネル検査を受ける際に、こうした利活用に99.7%の患者さんが同意されています。利活用に同意いただいた患者さんの協力と、その患者さんを治療している医師、医療者による臨床情報の登録作業の2つが、C-CAT活動の支えになっており、未来のがんゲノム医療の発展と向上につながっています。
プロフィール
河野隆志(こうのたかし)
1991年3月 京都大学大学院 薬学研究科修士課程 修了
1995年3月 東京大学大学院 医学研究科博士課程 修了
1995年5月 国立がんセンター研究所 生物学部 研究員
2000年4月 同 生物学部 室長
2010年10月 国立がん研究センター研究所 ゲノム生物学研究分野 分野長
2013年4月 国立がん研究センター先端医療開発センター ゲノムTR分野 分野長(併任)
2016年7月 東京慈恵会医科大学連携大学院教授(分子腫瘍学) (併任)
2018年6月 国立がん研究センターがんゲノム情報管理センター情報利活用戦略室 室長(併任)

