前立腺がんのリスク分類による初期治療の選択とは 監視療法、手術療法、放射線療法、ホルモン療法、フォーカルセラピー

2018.1 取材・文:柄川明彦
前立腺がんの治療に関する最新情報は、「前立腺がんを知る」をご参照ください。
前立腺がんの診断後の初期治療は、基本的にPSA値、がん組織の悪性度、がんの進展度を総合的に判定するリスク分類により、「監視療法」「手術療法」「放射線療法」「ホルモン療法」「フォーカルセラピー」が選択されます。実際の初期治療は、低中高リスクの違いだけでなく、患者さんの状態(年齢や健康)、希望なども加味しながら患者さんにあった選択がなされます。治療ごとの特徴やメリット、リスクを知ることで、自分にあった治療を見つけてください。
がんの広がりやリスク分類によって初期治療を選択
前立腺がんの治療法は多岐にわたっています。前立腺がんと診断がつき、まず行われる初期治療にも、いろいろな選択肢があります。そのがんが前立腺にとどまる限局性がんであれば、手術療法や放射線療法が選択できますし、場合によっては、監視療法やフォーカルセラピーが選択できるかもしれません。がんが周辺の組織や隣接する臓器にまで広がった局所進行がんにも、手術療法と放射線療法という選択肢があります。転移性がんになると、ホルモン療法や化学療法が選択されます。いずれの場合も、治療効果や合併症、患者さんの生活状況や希望を加えた治療法の選択が考慮されます。
初期治療として行われる可能性のある監視療法、手術療法、放射線療法、ホルモン療法、フォーカルセラピーについて、それぞれどのような治療法かを説明していきましょう。
病期別治療アルゴリズム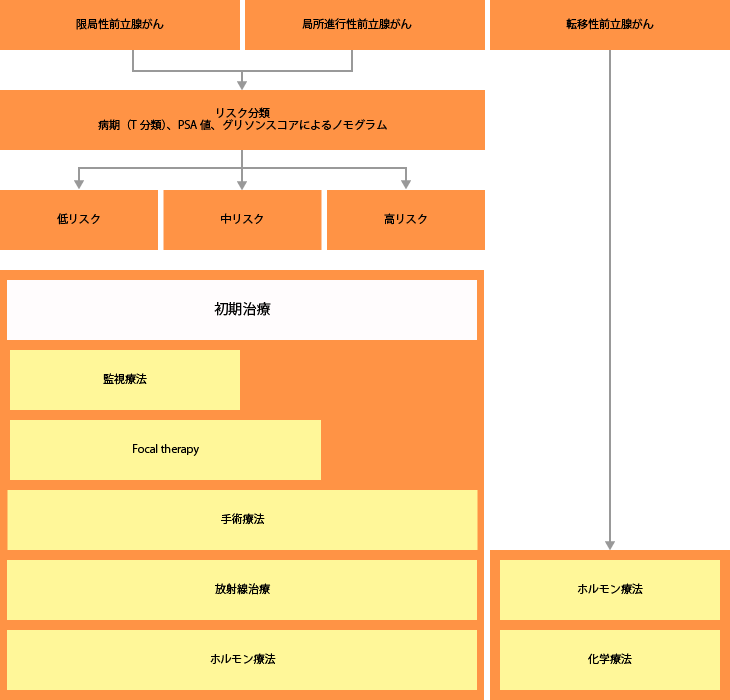
前立腺癌診療ガイドライン2016年版より作成
監視療法-生命予後に影響があるものないものを適切に見極める
監視療法は、がんを直接攻撃するような治療が必要になるまで治療をせず、定期的な観察を行うという方法です。基本的には年に1回の生検で経過を見て行き、治療が必要と判断できる検査結果が出た場合や、患者さんが治療を希望する場合には、治療を開始します。
監視療法が行われるようになったのは、PSA検診が普及して、早い段階の前立腺がんが見つかるようになったことが関係しています。前立腺がんは高齢者に多いため、早い段階のがんで、悪性度が低ければ、一生治療しなくてよいケースもあります。治療を受けたことで、がんが完治しても、排尿障害や性機能障害などの合併症が残ることがあります。そこで、できるだけ無駄な治療を回避するため、監視療法が行われるようになりました。
この治療に適しているのは、比較的高齢の患者さんで、限局性がんで、がんの悪性度が低く(グリソンスコアが6あるいは7程度)、PSAも比較的低く(10ng/ml以下)、臨床病期もT1~T2aくらいの場合です。MRI検査の結果、腫瘍が大きい場合は向きません。また、生検を行ったときに、陽性が何本あったか(陽性コア率)も重要です。たとえば12本の組織を採取した場合、監視療法に向いているのは、陽性が1~2本の場合です。
監視療法では定期的に生検を行います。生検による副作用はほとんどありませんが、患者さんにとって負担であることは確かです。生検時に麻酔を使う場合は、1泊程度の入院が必要になります。経直腸生検であれば、麻酔を使用せずに行うこともでき、その場合には日帰りも可能です。経会陰生検は、麻酔なしで行うのは難しいでしょう。
監視療法は不必要な治療を回避するのに役立ちますが、がんがあるとわかっていながら治療をしないことが、患者さんにとって精神的な負担となることがありため、こころのケアも大切です。
手術療法-エビデンスがある根治的治療。ロボット支援手術の普及で術後のQOLが改善
前立腺がん治療では、限局性がんでも局所進行がんでも手術療法の対象となり、前立腺すべてと精嚢を切除する前立腺全摘除術が行われます。ただし、一般的には75歳を過ぎた患者さんには勧められていません。
手術方法は、開腹手術、腹腔鏡下手術、ロボット支援手術という3つがあります。
最も古くから行われていたのが開腹手術で、術者が組織に触れることができるのがメリットです。下腹部を切開して行うのが一般的ですが、会陰部から切開する方法もあります。
腹腔鏡下手術は、数か所の小さな切開部から腹腔鏡と手術器具を挿入し、手術を行います。患部を拡大して見られることや、傷口が小さく出血が少ないため、患者さんの回復が早いのが特徴です。
ロボット支援手術は、腹腔鏡下手術でやるのと同じことを、手術用のロボットを使用して行います。手術器具の可動範囲が広く、小回りもきくので、狭い空間で精密な作業を行うのに適しています。技術的な面に関しては、ロボット支援手術が最も優れています。
手術の治療成績に関するデータはいろいろありますが、前立腺がんの根治性に関しては、ロボットを使用してもあまり変わりません。ただ、術後のQOLに関しては、ロボット支援手術のほうが優れているというデータが出ています。前立腺がんの手術後には、尿もれや性機能障害が起き、徐々に改善していきます。ロボット支援手術の場合、吻合が確実にできるため、術後に起きる尿失禁の回復が早いのです。また、性機能を残すための神経温存も、ロボットで行ったほうがうまくいき、回復率が高くなります。
前立腺がんの手術では、所属リンパ節の郭清を行います。その主な目的は、治療効果を高めることではなく、がんの転移がリンパ節に及んでいないかどうかを確認することです。画像検査では小さな転移まではわからないので、手術時にリンパ節を切除し、病理検査を行います。高リスクのがんに関しては、治療効果を高める目的で、もっと広い範囲のリンパ節を切除する拡大リンパ節郭清が行われることもあります。
放射線療法-手術と同等の治療成績。外照射と組織内照射という2つの方法がある
放射線療法には、体の外側から放射線を照射する外照射と、体内に線源を入れて内側から照射する組織内照射という方法があります。年齢による制限はなく、高齢の患者さんでも対象となります。
外照射
かつての外照射は、体の前後と左右方向からしか放射線を照射できず、照射野が箱型になるため、ボックス照射と呼ばれていました。その後、3D-CRT(3次元原体照射)という方法が登場し、いろいろな方向からの照射が可能になり、照射野は角がとれ丸みをおびた形になりました。しかし、一部をへこませることはできませんでしたが、コンピュータ技術の進歩でそれを可能にしたのが、IMRT(強度変調放射線治療)という方法です。前立腺は直腸と接していますが、IMRTなら直腸をよけて前立腺に放射線を照射できます。現在は、3D-CRTかIMRTが行われています。
照射法が進歩し、正常組織を避けて放射線を患部に集中できるようになったため、より多くの線量を照射できるようになりました。ボックス照射の時代は60数グレイ、3D-CRTになり70数グレイ、IMRTでは80グレイも可能になっています。照射できる線量が増えることで、治療効果も向上しています。
外照射は治療期間が長く、80グレイの場合、1日2グレイを40日間(1週5日間で8週間)照射します。
一般的には、外照射にはホルモン療法を併用します。ホルモン療法を併用する群と併用しない群を比較した臨床試験で、併用すると治療効果が高まることが明らかになっています。ホルモン療法によって、放射線に対する感受性が高まるとも言われています。特に高リスクと中リスクの場合、長期間のホルモン療法を併用することが推奨されています。
たとえば高リスクの場合は、放射線療法を開始する3か月前からホルモン療法を始め、その後放射線療法を併用し、さらにホルモン療法を続け、全体で2年間、中リスクの場合は、全体で9か月間行います。
治療が終了した直後の合併症として、排尿痛、頻尿などの排尿障害や便意切迫感などが時々起こりますが、手術療法のような尿失禁が生じないのが特徴です。晩期合併症として、治療後1年ほど経過してから、血尿、血便、頻尿や性機能障害などの合併症が現れ、QOLを低下させることがあります。
組織内照射
使用する線源によって、シード線源永久挿入小線源療法と高線量率組織内照射という2つの方法があります。広く行われているのは、比較的低い線量の線源を使用するシード線源永久挿入小線源療法です。
シード線源永久挿入小線源療法では、ヨード125という線源の入った小さなカプセル(直径0.8mm、長さ4.5mm)を前立腺の大きさに応じて60~120本を埋め込みます。半減期は60日ほどで、1年後には放射線は出なくなります。
低リスクと中リスクの一部に対しては、シード線源永久挿入小線源療法単独での治療が行われます。この場合、外照射に比べ、合併症が起こりにくいという特徴がありますが、治療直後に頻尿や排尿困難が起きます。
高リスクや中リスクに対しては、シード線源永久挿入小線源療法と外照射を併用する治療も行われています。外照射単独と比較した臨床試験では、併用療法のほうが優れていることが証明されています。ヨード125ではガンマ線、外照射ではエックス線が照射されるため、単純に計算はできませんが、シード線源永久挿入小線源療法と外照射を併用した場合の線量は、外照射だけの場合よりはるかに多くなります。
高線量率組織内照射は、強い放射線を出すイリジウム192という線源を使います。前立腺に針を通しておき、この中に線源を入れて移動させ、短時間だけ前立腺に照射します。1日2回行い、多くの場合、外照射を併用します。
ホルモン療法-前立腺がんを刺激する男性ホルモンを内科的に枯渇させる治療
前立腺がんは、精巣や副腎から分泌される男性ホルモンにより進行します。精巣を切除して抑える外科的去勢に対して、薬剤で内科的に去勢することで、がんの増殖を抑制する治療です。手術や放射線治療が難しい場合、放射線治療を補う場合、転移がある場合などに行われます。
男性ホルモンの分泌を抑えるために、LH-RHアゴニストやLH-RHアンタゴニストの注射薬が使われます。また、男性ホルモンが前立腺がんに作用するのを防ぐために、抗アンドロゲン作用の内服薬が使われます。
男性ホルモンを枯渇させるため副作用として、性機能への影響、循環器疾患のリスク、骨密度が低下することがあります。
フォーカルセラピー-前立腺を部分的に温存してQOLを保つ
前立腺全体に治療を加えるのではなく、病巣の部分だけを治療する、前立腺の半分を治療するというように、部分的に治療する方法です。治療方法はさまざまですが、代表的なものがHIFU(高密度焦点超音波)です。直腸に挿入した器具から超音波を発信し、それを前立腺に集中させ、高温にすることでがんを死滅させます。前立腺がんを根本的に治療するのには適していませんが、部分的に治療するのには向いています。合併症としては、排尿困難などの排尿障害があります。
前立腺全体に治療を加えると、精液の生成量が減るため、精液があまり出なくなります。これに不快な感覚を持つ患者さんが多く、フォーカルセラピーではそれが解消されます。性機能の温存はかなりの確率で可能です。
ただし、誰にでもできる治療ではありません。限局性がんであることに加え、解析度の高いMRI検査やマッピングバイオプシー(本数の多い生検でどこにがんがあるかを調べる)などで、前立腺内のがんの位置が正確にわかった場合には、選択されてもよい治療だといえるでしょう。
プロフィール
斉藤史郎(さいとうしろう)
1984年5月 慶應義塾大学医学部助手
1987年6月 慶應義塾大学医学部助手、泌尿器科チーフレジデント
1992年2月 米国Memorial Sloan-Kettering Cancer Center研究員
1997年3月 慶應義塾大学医学部講師
1997年4月 国立病院機構東京医療センター泌尿器科医長

