治療選択
非小細胞肺がん治療の選択
非小細胞肺がんでは、ステージ1、2と、3の一部まで切除手術が可能とされています。一方で、ステージ1や2でも、患者さんの全身状態がよくない、合併症がある、手術に耐えられる年齢ではないなど、手術が難しいと判断された場合は、放射線治療や化学放射線治療が選択される場合もあります。手術可能であれば、手術後、再発予防のために抗がん剤を投与する補助化学療法が行われる場合もあります。ステージ3や4で手術によりがんを完全に切除できないと判断された場合は、化学療法や放射線治療、化学療法と放射線治療を組み合わせた化学放射線療法のいずれかが選択されます。薬物療法は、細胞障害性の抗がん剤、分子標的薬、免疫チェックポイント阻害薬などが、患者さんの状態や年齢、遺伝子変異など、さまざまな要素を検討して選択されます。
ステージ1A/Bの非小細胞肺がんの治療選択
ステージ1A/Bの非小細胞肺がんと診断された場合、標準的な手術の可否が判定されます、手術可能と判定された場合は、標準的な手術が推奨されています。
ステージ1A1~2の非小細胞肺がんに対しては、縮小手術も推奨されています。充実成分最大径に対し腫瘍最大径の比率が0.25%以下の肺野部(気管支の末梢から肺胞のある肺の奥の部分)の末梢非小細胞肺がんでは区域切除または楔状切除が、0.5%を超える場合は区域切除または肺葉切除が、それぞれ推奨されています。ステージ1A3~2の非小細胞肺がんに対しては、肺葉以上の切除が推奨されています。
ステージ1の非小細胞肺がんで手術は可能でも肺葉以上の切除が不可能な場合は、縮小手術として区域切除または楔状切除が検討されます。また、医学的な理由で肺葉以上の切除が不可能な場合もしくは手術を患者さんが希望しない場合は、根治的放射線治療が推奨されています。
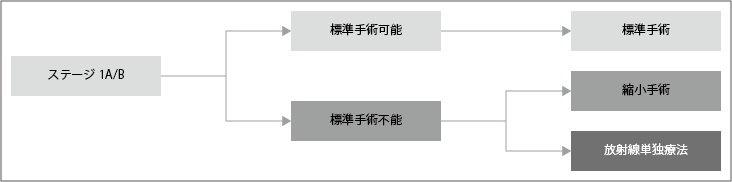
参考:日本肺癌学会. 肺癌診療ガイドライン ―悪性胸膜中皮腫・胸腺腫瘍含む― 2023年版.II.非小細胞肺癌(NSCLC).非小細胞肺癌の樹形図より作成
ステージ2A/B(肺尖部胸壁浸潤がんを除く)の非小細胞肺がんの治療選択
ステージ2A/B(肺尖部胸壁浸潤がんを除く)の非小細胞肺がんと診断された場合、手術可能かどうかが判定されます。手術可能な場合は、肺葉切除以上の切除と肺門・縦隔のリンパ節郭清が推奨されています。手術不能と判定された全身状態が0~1の患者さんに対しては、化学放射線治療が推奨されています。化学療法が併用できない患者さんに対しては、単独の放射線治療が推奨されています。
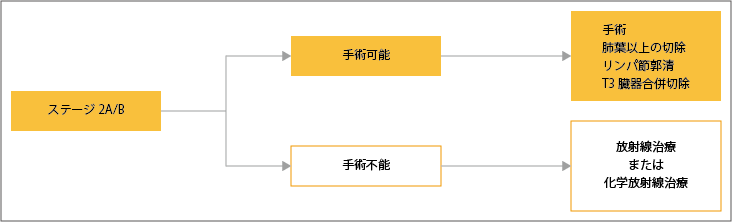
参考:日本肺癌学会. 肺癌診療ガイドライン ―悪性胸膜中皮腫・胸腺腫瘍含む― 2023年版.II.非小細胞肺癌(NSCLC).非小細胞肺癌の樹形図より作成
ステージ2B(肺尖部胸壁浸潤がん)/3Aの非小細胞肺がんの治療選択
ステージ2B(肺尖部胸壁浸潤がん)/3Aの非小細胞肺がんと診断された場合、手術可能かどうかが判定されます。手術可能な場合は、必要に応じて術前治療が行われます。ステージ3(T4N0-1)の場合は、手術が考慮されます。手術を行う場合は、肺門部・縦隔リンパ節郭清が推奨されています。ステージ3(T3N0-1M0)の胸壁浸潤がんや心膜に浸潤している場合は、胸壁合併切除が推奨されています。
手術不能の場合は、ステージ3B/Cに準じた治療が行われます。
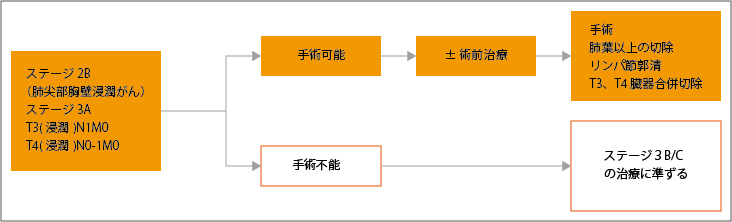
参考:日本肺癌学会. 肺癌診療ガイドライン ―悪性胸膜中皮腫・胸腺腫瘍含む― 2023年版.II.非小細胞肺癌(NSCLC).非小細胞肺癌の樹形図より作成
ステージ3A-N2/B-N2の非小細胞肺がんの治療選択
切除可能なステージ3A-N2に対しては、術前治療として化学放射線治療が考慮されます。術前治療後は、肺葉切除以上の手術を行う場合は、肺門部・縦隔リンパ節郭清、胸壁合併切除が行われます。
切除不能の場合は、ステージ3B/Cに準じた治療が行われます。
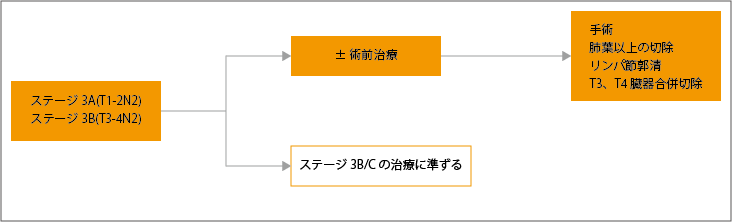
参考:日本肺癌学会. 肺癌診療ガイドライン ―悪性胸膜中皮腫・胸腺腫瘍含む― 2023年版.II.非小細胞肺癌(NSCLC).非小細胞肺癌の樹形図より作成
ステージ3B/Cの非小細胞肺がんの治療選択
ステージ3B/Cの非小細胞肺がんと診断された場合、根治的放射線治療が可能かどうかが判定されます。放射線治療が可能と判定された場合は、さらに化学療法が可能かどうかが判定され、化学療法併用が可能な場合は、化学放射線治療、不能な場合は放射線単独治療が選択されます。
放射線治療が不能と判定された場合は、ステージ4の一次治療に準じた治療が行われます。
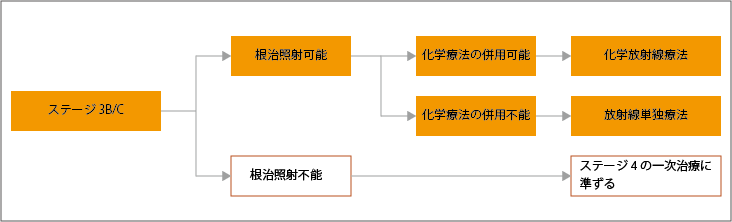
参考:日本肺癌学会. 肺癌診療ガイドライン ―悪性胸膜中皮腫・胸腺腫瘍含む― 2023年版.II.非小細胞肺癌(NSCLC).非小細胞肺癌の樹形図より作成
ステージ4の非小細胞肺がんの治療選択
ステージ4の非小細胞肺がんと診断された場合は、薬物療法が推奨されています。薬物療法を行うにあたり、原因遺伝子となるドライバー遺伝子変異や転座などを調べる検査が行われます。ドライバー遺伝子変異/転座陽性の場合は、「EGFR遺伝子変異」「ALK融合遺伝子」「ROS1融合遺伝子」「BRAF遺伝子変異」「MET遺伝子変異」「RET融合遺伝子」「NTRK融合遺伝子」「KRAS遺伝子変異」「HER2遺伝子変異」などの遺伝子変異(遺伝子の変化)を特定し、各ドライバー遺伝子に対する分子標的薬による治療が推奨されています。
ドライバー遺伝子変異/転座陰性の場合は、PD-L1検査により、「PD-L1 TPS 1%未満」「PD-L1 TPS 1~49%」「PD-L1 TPS 50%以上」の3つのサブグループに分類し、それぞれのTPSに応じた治療が選択されます。
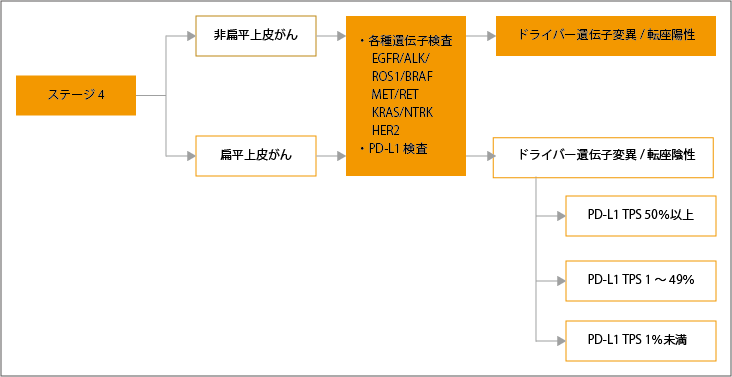
参考:日本肺癌学会. 肺癌診療ガイドライン ―悪性胸膜中皮腫・胸腺腫瘍含む― 2023年版.II.非小細胞肺癌(NSCLC).非小細胞肺癌の樹形図より作成
EGFR遺伝子変異陽性の治療選択
ステージ4のEGFR遺伝子変異(エクソン19欠失、L858R変異)陽性非小細胞肺がんでは、全身状態により一次治療薬が異なります。全身状態が0~1の場合は、オシメルチニブが推奨され、ゲフィチニブ+カルボプラチン+ペメトレキセド併用療法、エルロチニブ+血管新生阻害薬、ダコミチニブも治療選択として考慮されます。
全身状態が2の場合は、ゲフィチニブもしくはエルロチニブによる単剤療法が推奨されています。
全身状態が3~4の場合は、ゲフィチニブ単剤療法が推奨されています。
EGFRエクソン18~21遺伝子変異(E709X、G719X、S768I、P848L、L861Q、エクソン19挿入変異など)の場合は、ゲフィチニブ、エルロチニブ、アファチニブ、オシメルチニブのいずれかの単剤療法が推奨されています。また、エクソン20挿入変異に対しては、EGFR阻害薬による治療は行わないことが推奨されています。
一次治療でEGFR阻害薬の耐性または増悪後に、T790M変異陽性となった場合で、一次治療としてオシメルチニブを用いていなければ、オシメルチニブが推奨されています。
二次治療以降は、細胞傷害性抗がん薬と免疫チェックポイント阻害薬による治療が、患者さんの病態により選択されます。
全身状態0~1の患者さんに対しては、PD-L1の発現率(TPS)により、治療が異なります。TPS 50%以上では、ペムブロリズマブまたはアテゾリズマブ単剤が推奨されています。また、プラチナ製剤併用療法+PD-1/PD-L1阻害薬併用療法も推奨さています。しかし、PD-1/PD-L1阻害薬+CTLA-4阻害薬併用療法を推奨するだけの根拠はまだ明確になっていません。
TPS 1~49%では、プラチナ製剤併用療法+PD-1/PD-L1阻害薬併用療法が推奨さています。また、PD-1/PD-L1阻害薬+CTLA-4阻害薬併用療法も治療選択肢の1つとして考慮されていますが、ペムブロリズマブ単剤を推奨するだけの根拠はまだ明確になっていません。
TPS 1%未満では、プラチナ製剤併用療法+PD-1/PD-L1阻害薬併用療法が推奨さています。また、PD-1/PD-L1阻害薬+CTLA-4阻害薬併用療法も治療選択肢の1つとして考慮されています。
全身状態2の患者さんに対しては、細胞傷害性抗がん薬が推奨されています。また、TPS 50%以上の患者さんに対しては、ペムブロリズマブ単剤も治療選択の1つとして考慮されています。しかし、プラチナ製剤併用療法に免疫チェックポイント阻害薬併用療法は、推奨するだけの根拠が、まだ明確になっていません。
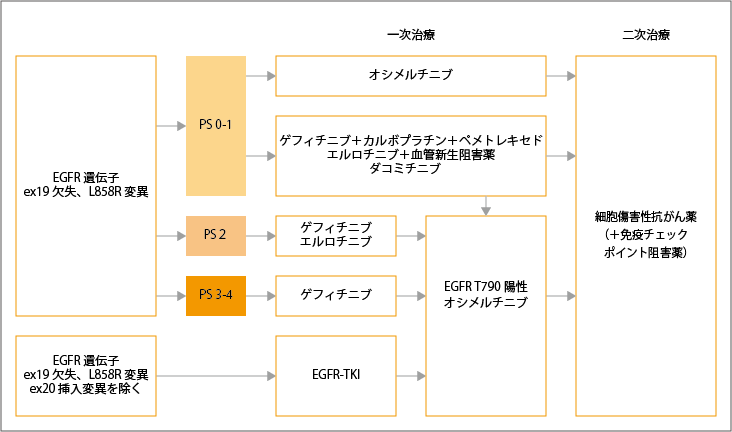
参考:日本肺癌学会. 肺癌診療ガイドライン ―悪性胸膜中皮腫・胸腺腫瘍含む― 2023年版.II.非小細胞肺癌(NSCLC).非小細胞肺癌の樹形図より作成
ALK融合遺伝子陽性の治療選択
ステージ4のALK癒合遺伝子陽性非小細胞肺がんでは、全身状態により一次治療薬が異なります。全身状態が0~1の場合は、アレクチニブが推奨され、ブリグチニブとロルラチニブも治療選択として考慮されます。
全身状態が2~4の場合は、アレクチニブが推奨されています。
二次治療以降は、細胞傷害性抗がん薬と免疫チェックポイント阻害薬による治療が、患者さんの病態により選択されます。
アレクチニブ耐性または増悪後の全身状態0~2の二次治療では、ブリグチニブ、ロルラチニブが検討されます。
全身状態0~1の患者さんに対しては、PD-L1の発現率(TPS)により、治療が異なります。TPS 50%以上では、ペムブロリズマブまたはアテゾリズマブ単剤が推奨されています。また、プラチナ製剤併用療法+PD-1/PD-L1阻害薬併用療法も推奨さています。しかし、PD-1/PD-L1阻害薬+CTLA-4阻害薬併用療法を推奨するだけの根拠はまだ明確になっていません。
TPS 1~49%では、プラチナ製剤併用療法+PD-1/PD-L1阻害薬併用療法が推奨さています。また、PD-1/PD-L1阻害薬+CTLA-4阻害薬併用療法も治療選択肢の1つとして考慮されていますが、ペムブロリズマブ単剤を推奨するだけの根拠はまだ明確になっていません。
TPS 1%未満では、プラチナ製剤併用療法+PD-1/PD-L1阻害薬併用療法が推奨さています。また、PD-1/PD-L1阻害薬+CTLA-4阻害薬併用療法も治療選択肢の1つとして考慮されています。
全身状態2の患者さんに対しては、細胞傷害性抗がん薬が推奨されています。また、TPS 50%以上の患者さんに対しては、ペムブロリズマブ単剤も治療選択の1つとして考慮されています。しかし、プラチナ製剤併用療法に免疫チェックポイント阻害薬併用療法を推奨するだけの根拠は、まだ明確になっていません。
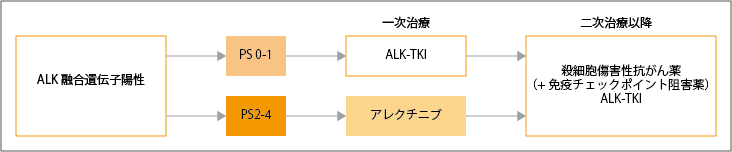
参考:日本肺癌学会. 肺癌診療ガイドライン ―悪性胸膜中皮腫・胸腺腫瘍含む― 2023年版.II.非小細胞肺癌(NSCLC).非小細胞肺癌の樹形図より作成
ROS1融合遺伝子陽性の治療選択
ステージ4のROS1融合遺伝子陽性の非小細胞肺がんでは、一次治療としてクリゾチニブまたはエヌトレクチニブのいずれかが推奨されています。
二次治療以降は、細胞傷害性抗がん薬と免疫チェックポイント阻害薬による治療が、患者さんの病態により選択されます。
全身状態0~1の患者さんに対しては、PD-L1の発現率(TPS)により、治療が異なります。TPS 50%以上では、ペムブロリズマブまたはアテゾリズマブ単剤が推奨されています。また、プラチナ製剤併用療法+PD-1/PD-L1阻害薬併用療法も推奨さています。しかし、PD-1/PD-L1阻害薬+CTLA-4阻害薬併用療法を推奨するだけの根拠はまだ明確になっていません。
TPS 1~49%では、プラチナ製剤併用療法+PD-1/PD-L1阻害薬併用療法が推奨さています。また、PD-1/PD-L1阻害薬+CTLA-4阻害薬併用療法も治療選択肢の1つとして考慮されていますが、ペムブロリズマブ単剤を推奨するだけの根拠はまだ明確になっていません。
TPS 1%未満では、プラチナ製剤併用療法+PD-1/PD-L1阻害薬併用療法が推奨さています。また、PD-1/PD-L1阻害薬+CTLA-4阻害薬併用療法も治療選択肢の1つとして考慮されています。
全身状態2の患者さんに対しては、細胞傷害性抗がん薬が推奨されています。また、TPS 50%以上の患者さんに対しては、ペムブロリズマブ単剤も治療選択の1つとして考慮されています。しかし、プラチナ製剤併用療法に免疫チェックポイント阻害薬併用療法を推奨するだけの根拠は、まだ明確になっていません。

参考:日本肺癌学会. 肺癌診療ガイドライン ―悪性胸膜中皮腫・胸腺腫瘍含む― 2023年版.II.非小細胞肺癌(NSCLC).非小細胞肺癌の樹形図より作成
BRAF遺伝子V600E変異陽性の治療選択
ステージ4のBRAF遺伝子V600E変異陽性の非小細胞肺がんでは、一次治療としてダブラフェニブ+トラメチニブ併用療法が推奨されています。
二次治療以降は、細胞傷害性抗がん薬と免疫チェックポイント阻害薬による治療が、患者さんの病態により選択されます。
全身状態0~1の患者さんに対しては、PD-L1の発現率(TPS)により、治療が異なります。TPS 50%以上では、ペムブロリズマブまたはアテゾリズマブ単剤が推奨されています。また、プラチナ製剤併用療法+PD-1/PD-L1阻害薬併用療法も推奨さています。しかし、PD-1/PD-L1阻害薬+CTLA-4阻害薬併用療法を推奨するだけの根拠はまだ明確になっていません。
TPS 1~49%では、プラチナ製剤併用療法+PD-1/PD-L1阻害薬併用療法が推奨さています。また、PD-1/PD-L1阻害薬+CTLA-4阻害薬併用療法も治療選択肢の1つとして考慮されていますが、ペムブロリズマブ単剤を推奨するだけの根拠はまだ明確になっていません。
TPS 1%未満では、プラチナ製剤併用療法+PD-1/PD-L1阻害薬併用療法が推奨さています。また、PD-1/PD-L1阻害薬+CTLA-4阻害薬併用療法も治療選択肢の1つとして考慮されています。
全身状態2の患者さんに対しては、細胞傷害性抗がん薬が推奨されています。また、TPS 50%以上の患者さんに対しては、ペムブロリズマブ単剤も治療選択の1つとして考慮されています。しかし、プラチナ製剤併用療法に免疫チェックポイント阻害薬併用療法を推奨するだけの根拠は、まだ明確になっていません。

参考:日本肺癌学会. 肺癌診療ガイドライン ―悪性胸膜中皮腫・胸腺腫瘍含む― 2023年版.II.非小細胞肺癌(NSCLC).非小細胞肺癌の樹形図より作成
MET遺伝子変異陽性の治療選択
ステージ4のMET遺伝子変異陽性の非小細胞肺がんでは、一次治療をしてテポチニブまたはカプマチニブいずれかが推奨されています。
二次治療以降は、細胞傷害性抗がん薬と免疫チェックポイント阻害薬による治療が、患者さんの病態により選択されます。
全身状態0~1の患者さんに対しては、PD-L1の発現率(TPS)により、治療が異なります。TPS 50%以上では、ペムブロリズマブまたはアテゾリズマブ単剤が推奨されています。また、プラチナ製剤併用療法+PD-1/PD-L1阻害薬併用療法も推奨さています。しかし、PD-1/PD-L1阻害薬+CTLA-4阻害薬併用療法を推奨するだけの根拠はまだ明確になっていません。
TPS 1~49%では、プラチナ製剤併用療法+PD-1/PD-L1阻害薬併用療法が推奨さています。また、PD-1/PD-L1阻害薬+CTLA-4阻害薬併用療法も治療選択肢の1つとして考慮されていますが、ペムブロリズマブ単剤を推奨するだけの根拠はまだ明確になっていません。
TPS 1%未満では、プラチナ製剤併用療法+PD-1/PD-L1阻害薬併用療法が推奨さています。また、PD-1/PD-L1阻害薬+CTLA-4阻害薬併用療法も治療選択肢の1つとして考慮されています。
全身状態2の患者さんに対しては、細胞傷害性抗がん薬が推奨されています。また、TPS 50%以上の患者さんに対しては、ペムブロリズマブ単剤も治療選択の1つとして考慮されています。しかし、プラチナ製剤併用療法に免疫チェックポイント阻害薬併用療法を推奨するだけの根拠は、まだ明確になっていません。

参考:日本肺癌学会. 肺癌診療ガイドライン ―悪性胸膜中皮腫・胸腺腫瘍含む― 2023年版.II.非小細胞肺癌(NSCLC).非小細胞肺癌の樹形図より作成
RET融合遺伝子陽性の治療選択
ステージ4のRET融合遺伝子陽性の非小細胞肺がんでは、一次治療としてセルペルカチニブが推奨されています。
二次治療以降は、細胞傷害性抗がん薬と免疫チェックポイント阻害薬による治療が、患者さんの病態により選択されます。
全身状態0~1の患者さんに対しては、PD-L1の発現率(TPS)により、治療が異なります。TPS 50%以上では、ペムブロリズマブまたはアテゾリズマブ単剤が推奨されています。また、プラチナ製剤併用療法+PD-1/PD-L1阻害薬併用療法も推奨さています。しかし、PD-1/PD-L1阻害薬+CTLA-4阻害薬併用療法を推奨するだけの根拠はまだ明確になっていません。
TPS 1~49%では、プラチナ製剤併用療法+PD-1/PD-L1阻害薬併用療法が推奨さています。また、PD-1/PD-L1阻害薬+CTLA-4阻害薬併用療法も治療選択肢の1つとして考慮されていますが、ペムブロリズマブ単剤を推奨するだけの根拠はまだ明確になっていません。
TPS 1%未満では、プラチナ製剤併用療法+PD-1/PD-L1阻害薬併用療法が推奨さています。また、PD-1/PD-L1阻害薬+CTLA-4阻害薬併用療法も治療選択肢の1つとして考慮されています。
全身状態2の患者さんに対しては、細胞傷害性抗がん薬が推奨されています。また、TPS 50%以上の患者さんに対しては、ペムブロリズマブ単剤も治療選択の1つとして考慮されています。しかし、プラチナ製剤併用療法に免疫チェックポイント阻害薬併用療法を推奨するだけの根拠は、まだ明確になっていません。

参考:日本肺癌学会. 肺癌診療ガイドライン ―悪性胸膜中皮腫・胸腺腫瘍含む― 2023年版.II.非小細胞肺癌(NSCLC).非小細胞肺癌の樹形図より作成
NTRK融合遺伝子陽性の治療選択
ステージ4のNTRK融合遺伝子陽性の非小細胞肺がんでは、一次治療としてドライバー遺伝子 変異/転座陰性の初回治療に準じた治療が推奨されています。
全身状態0~1の患者さんに対しては、PD-L1の発現率(TPS)により、治療が異なります。TPS 50%以上では、ペムブロリズマブまたはアテゾリズマブ単剤が推奨されています。また、プラチナ製剤併用療法+PD-1/PD-L1阻害薬併用療法も推奨さています。しかし、PD-1/PD-L1阻害薬+CTLA-4阻害薬併用療法を推奨するだけの根拠はまだ明確になっていません。
TPS 1~49%では、プラチナ製剤併用療法+PD-1/PD-L1阻害薬併用療法が推奨さています。また、PD-1/PD-L1阻害薬+CTLA-4阻害薬併用療法も治療選択肢の1つとして考慮されていますが、ペムブロリズマブ単剤を推奨するだけの根拠はまだ明確になっていません。
TPS 1%未満では、プラチナ製剤併用療法+PD-1/PD-L1阻害薬併用療法が推奨さています。また、PD-1/PD-L1阻害薬+CTLA-4阻害薬併用療法も治療選択肢の1つとして考慮されます。
全身状態2の患者さんに対しては、細胞傷害性抗がん薬が推奨されています。また、TPS 50%以上の患者さんに対しては、ペムブロリズマブ単剤も治療選択の1つとして考慮されています。しかし、プラチナ製剤併用療法に免疫チェックポイント阻害薬併用療法を推奨するだけの根拠は、まだ明確になっていません。
二次治療以降では、エヌトレクチニブまたはラロトレクチニブのいずれかが推奨されています。

参考:日本肺癌学会. 肺癌診療ガイドライン ―悪性胸膜中皮腫・胸腺腫瘍含む― 2023年版.II.非小細胞肺癌(NSCLC).非小細胞肺癌の樹形図より作成
KRAS遺伝子変異陽性の治療選択
ステージ4のKRAS遺伝子変異陽性の非小細胞肺がんでは、一次治療としてドライバー遺伝子変異/転座陰性の初回治療に準じた治療が推奨されています。
全身状態0~1の患者さんに対しては、PD-L1の発現率(TPS)により、治療が異なります。TPS 50%以上では、ペムブロリズマブまたはアテゾリズマブ単剤が推奨されています。また、プラチナ製剤併用療法+PD-1/PD-L1阻害薬併用療法も推奨さています。しかし、PD-1/PD-L1阻害薬+CTLA-4阻害薬併用療法を推奨するだけの根拠はまだ明確になっていません。
TPS 1~49%では、プラチナ製剤併用療法+PD-1/PD-L1阻害薬併用療法が推奨さています。また、PD-1/PD-L1阻害薬+CTLA-4阻害薬併用療法も治療選択肢の1つとして考慮されていますが、ペムブロリズマブ単剤を推奨するだけの根拠はまだ明確になっていません。
TPS 1%未満では、プラチナ製剤併用療法+PD-1/PD-L1阻害薬併用療法が推奨さています。また、PD-1/PD-L1阻害薬+CTLA-4阻害薬併用療法も治療選択肢の1つとして考慮されています。
全身状態2の患者さんに対しては、細胞傷害性抗がん薬が推奨されています。また、TPS 50%以上の患者さんに対しては、ペムブロリズマブ単剤も治療選択の1つとして考慮されています。しかし、プラチナ製剤併用療法に免疫チェックポイント阻害薬併用療法を推奨するだけの根拠は、まだ明確になっていません。
二次治療以降では、ソトラシブが推奨されています。

参考:日本肺癌学会. 肺癌診療ガイドライン ―悪性胸膜中皮腫・胸腺腫瘍含む― 2023年版.II.非小細胞肺癌(NSCLC).非小細胞肺癌の樹形図より作成
HER2遺伝子変異陽性の治療選択
ステージ4のHER2遺伝子変異陽性の非小細胞肺がんでは、一次治療としてドライバー遺伝子変異/転座陰性の初回治療に準じた治療が推奨されています。
全身状態0~1の患者さんに対しては、PD-L1の発現率(TPS)により、治療が異なります。TPS 50%以上では、ペムブロリズマブまたはアテゾリズマブ単剤が推奨されています。また、プラチナ製剤併用療法+PD-1/PD-L1阻害薬併用療法も推奨さています。しかし、PD-1/PD-L1阻害薬+CTLA-4阻害薬併用療法を推奨するだけの根拠はまだ明確になっていません。
TPS 1~49%では、プラチナ製剤併用療法+PD-1/PD-L1阻害薬併用療法が推奨さています。また、PD-1/PD-L1阻害薬+CTLA-4阻害薬併用療法も治療選択肢の1つとして考慮されていますが、ペムブロリズマブ単剤を推奨するだけの根拠はまだ明確になっていません。
TPS 1%未満では、プラチナ製剤併用療法+PD-1/PD-L1阻害薬併用療法が推奨さています。また、PD-1/PD-L1阻害薬+CTLA-4阻害薬併用療法も治療選択肢の1つとして考慮されています。
全身状態2の患者さんに対しては、細胞傷害性抗がん薬が推奨されています。また、TPS 50%以上の患者さんに対しては、ペムブロリズマブ単剤も治療選択の1つとして考慮されています。しかし、プラチナ製剤併用療法に免疫チェックポイント阻害薬併用療法を推奨するだけの根拠は、まだ明確になっていません。
二次治療以降では、トラスツズマブ デルクステカンが推奨されています。

参考:日本肺癌学会. 肺癌診療ガイドライン ―悪性胸膜中皮腫・胸腺腫瘍含む― 2023年版.II.非小細胞肺癌(NSCLC).非小細胞肺癌の樹形図より作成
ドライバー遺伝子変異/転座陰性の治療選択
ドライバー遺伝子変異/転座陰性の非小細胞肺がんでは、PD-L1の発現率(TPS)により、「TPS 50%以上」「TPS 1~49%」「TPS 1%未満」に分類され、治療が選択されます。
PD-L1発現率 TPS 50%以上の治療選択
TPS 50%以上では、全身状態により治療選択が異なります。
全身状態0~1の患者さんに対する一次治療では、ペムブロリズマブまたはアテゾリズマブ単剤が推奨されています。また、プラチナ製剤併用療法+PD-1/PD-L1阻害薬併用療法も推奨さています。しかし、PD-1/PD-L1阻害薬+CTLA-4阻害薬併用療法を推奨するだけの根拠はまだ明確になっていません。
全身状態2の患者さん対する一次治療では、細胞傷害性抗がん薬が推奨されています。またペムブロリズマブ単剤も治療選択肢の1つとして考慮されています。しかし、プラチナ製剤併用療法に免疫チェックポイント阻害薬併用療法を推奨するだけの根拠は、まだ明確になっていません。
全身状態3~4の患者さんでは、薬物療法は推奨されていません。
全身状態0~1の患者さんに対する二次治療では、ドセタキセル±ラムシルマブ併用療法、ペメトレキセド単剤、S-1単剤、ナブパクリタキセル単剤のいずれかが推奨されています。ラムシルマブ適応に関しては、75歳以上、全身状態2の患者さんに対してはドセタキセルとの併用を行わないように推奨されています。
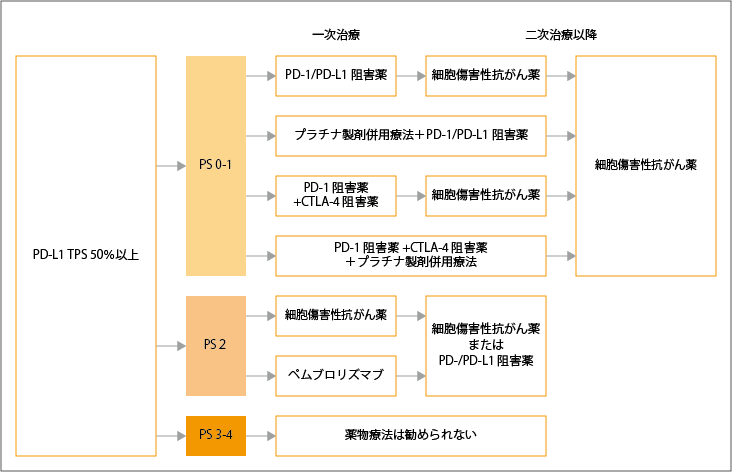
参考:日本肺癌学会. 肺癌診療ガイドライン ―悪性胸膜中皮腫・胸腺腫瘍含む― 2023年版.II.非小細胞肺癌(NSCLC).非小細胞肺癌の樹形図より作成
PD-L1発現率 TPS 1~49%の治療選択
TPS 1~49%では、全身状態により治療選択が異なります。
全身状態0~1の患者さんに対する一次治療では、プラチナ製剤併用療法+PD-1/PD-L1阻害薬併用療法が推奨さています。また、PD-1/PD-L1阻害薬+CTLA-4阻害薬+プラチナ製剤併用療法も治療選択肢の1つとして考慮されています。しかし、ペムブロリズマブ単剤を推奨するだけの根拠はまだ明確になっていません。
全身状態2の患者さん対する一次治療では、細胞傷害性抗がん薬が推奨されています。しかし、プラチナ製剤併用療法に免疫チェックポイント阻害薬併用療法は、推奨するだけの根拠が、まだ明確になっていません。
全身状態3~4の患者さんでは、薬物療法は推奨されていません。
全身状態0~1の患者さんに対する二次治療では、ドセタキセル±ラムシルマブ併用療法、ペメトレキセド単剤、S-1単剤、ナブパクリタキセル単剤のいずれかが推奨されています。ラムシルマブ適応に関しては、75歳以上、全身状態2の患者さんに対してはドセタキセルとの併用を行わないように推奨されています。
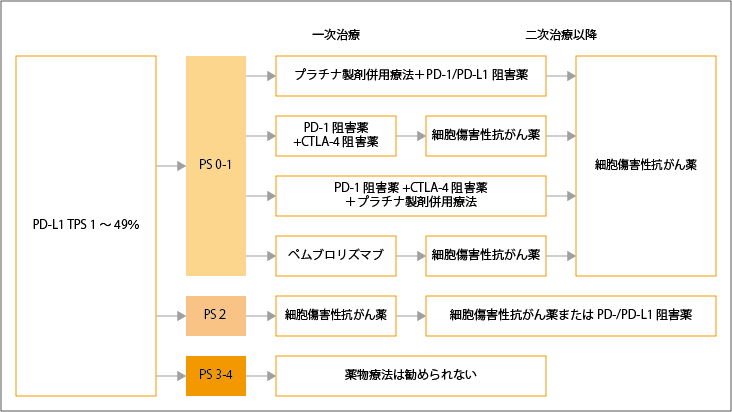
参考:日本肺癌学会. 肺癌診療ガイドライン ―悪性胸膜中皮腫・胸腺腫瘍含む― 2023年版.II.非小細胞肺癌(NSCLC).非小細胞肺癌の樹形図より作成
PD-L1発現率 TPS 1%未満の治療選択
TPS 1%未満では、全身状態により治療選択が異なります。
全身状態0~1の患者さんに対する一次治療では、プラチナ製剤併用療法+PD-1/PD-L1阻害薬併用療法が推奨さています。また、PD-1/PD-L1阻害薬+CTLA-4阻害薬+プラチナ製剤併用療法も治療選択肢の1つとして考慮されています。
全身状態2の患者さん対する一次治療では、細胞傷害性抗がん薬が推奨されています。しかし、プラチナ製剤併用療法に免疫チェックポイント阻害薬併用療法は、推奨するだけの根拠が、まだ明確になっていません。
全身状態3~4の患者さんでは、薬物療法は推奨されていません。
全身状態0~1の患者さんに対する二次治療では、ドセタキセル±ラムシルマブ併用療法、ペメトレキセド単剤、S-1単剤、ナブパクリタキセル単剤のいずれかが推奨されています。ラムシルマブ適応に関しては、75歳以上、全身状態2の患者さんに対してはドセタキセルとの併用を行わないように推奨されています。
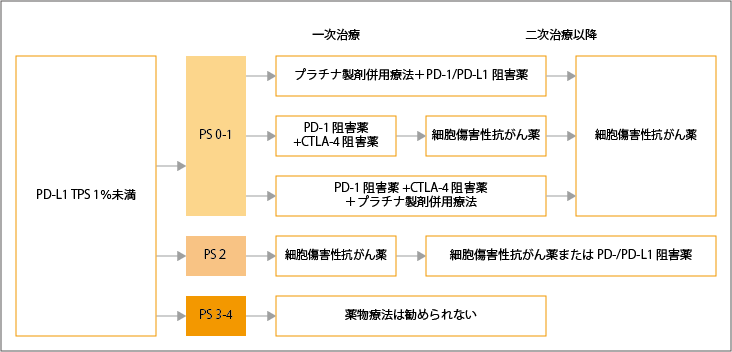
参考:日本肺癌学会. 肺癌診療ガイドライン ―悪性胸膜中皮腫・胸腺腫瘍含む― 2023年版.II.非小細胞肺癌(NSCLC).非小細胞肺癌の樹形図より作成
小細胞肺がん治療の選択
小細胞肺がんは、ステージ分類のほかに「限局型」と「進展型」による分類も行われ、治療選択が検討されます。限局型は、病巣が片側の胸腔と反対側の縦隔や鎖骨上窩リンパ節までに限られており、悪性胸水や心のう水がみられないタイプで、ステージ1~3です。進展型は、「限局型」の範囲を超えて進行しているタイプのことをいいます。
小細胞肺がんは、進行が速い一方、抗がん剤による化学療法がよく効くという特徴があります。
がんが肺にとどまり大きさが5cm以下の限局型小細胞肺がんのステージ1では、切除できるなら手術と、術後補助化学療法が行われます。医学的な理由で手術ができないステージ1もしくは2Aでは、定位放射線治療も治療選択として考慮されます。
手術ができないステージ1やステージ2以降で、全身状態(Performance Status:PS)が0~2の患者さんでは、化学療法と放射線治療を組み合わせて同時に行う化学放射線療法が推奨されます。PSが3の患者さんに対しては、化学療法が検討されます。PS4の患者さんでは、治療によりPSが改善する可能性があれば化学療法が考慮されますが、安全性に配慮して緩和ケアも検討されます。
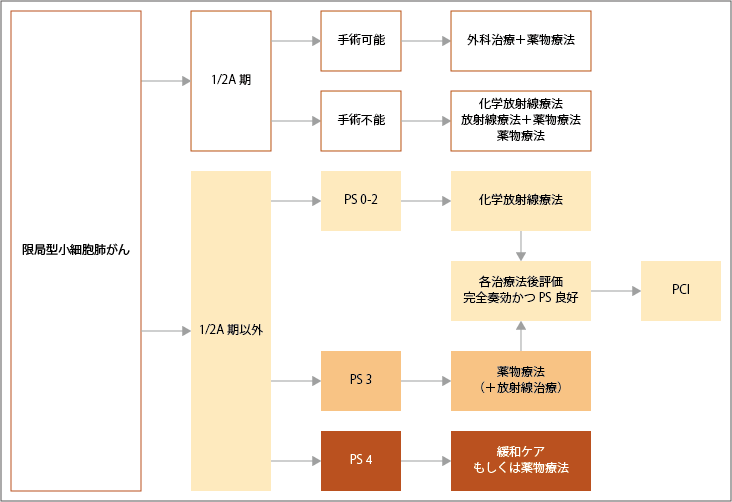
参考:日本肺癌学会. 肺癌診療ガイドライン ―悪性胸膜中皮腫・胸腺腫瘍含む― 2023年版.III.小細胞肺癌(SCLC).1限局型小細胞肺癌の樹形図より作成
進展型小細胞肺がんでは、PSにより治療が選択されます。PS0~1の患者さんに対しては、プラチナ製剤+PD-L1阻害薬併用療法が推奨されています。
PS0~2で70歳以下の患者さんでは、シスプラチン+イリノテカン併用療法が推奨されますが、71歳以上の患者さんに対する一次治療は、シスプラチンの一括投与が可能なら、シスプラチン+エトポシド併用療法が推奨されています。シスプラチンの一括投与が困難な場合は、カルボプラチン+エトポシド併用療法、あるいはシスプラチンを分割投与するシスプラチン+エトポシド併用療法が推奨されています。
PS0~1の進展型小細胞肺がん患者さんに対しては、プラチナ製剤+エトポシド+PD-L1阻害薬併用療法が推奨されています。
PS3の患者さんに対して、カルボプラチン+エトポシド併用療法、あるいはシスプラチンを分割投与するシスプラチン+エトポシド併用療法が考慮されています。PSが4の患者さんには、化学療法を行わないように提案され、緩和ケアが検討されます。
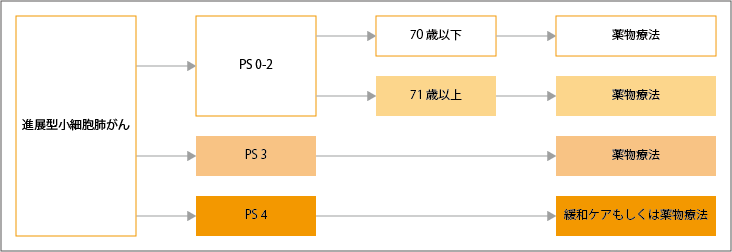
参考:日本肺癌学会. 肺癌診療ガイドライン ―悪性胸膜中皮腫・胸腺腫瘍含む― 2023年版.III.小細胞肺癌(SCLC).1進展型小細胞肺癌の樹形図より作成
再発・転移
がんの再発とは、治療によりいったんがんがなくなったのに、再びがんが発生することをいいます。同じ部位に再発したり、離れた別の部位に再発することもあります。多くの場合、初期治療の段階で、目に見えなかったり、検査で見つけられなかった小さながん細胞が、すでに転移していたために起こります。そのため、再発非小細胞肺がんの基本的な治療は、ステージ4の治療に準じて行われます。一般的に薬物療法が中心となりますが、再発した場所や大きさ、個数、症状などにより、手術や放射線治療が検討されることもあり、患者さんの個別の状態で治療方針が決められます。
小細胞肺がんの再発
小細胞肺がんの再発では、初期治療で行った抗がん剤の治療効果や再発までの期間が参考にされます。
再発までの期間が60~90日以上と長い患者さん(sensitive relapse)では、化学療法が行われます。sensitive relapseの患者さんに対しては、現在標準治療はありませんが、全身状態を考慮した上で、化学療法が検討されます。
がんの転移とは、小さながん細胞がリンパ液や血液の流れにのり別の臓器に運ばれ、そこで成長して発生することをいいます。肺がんの転移しやすい部位は、リンパ節、脳、肝臓、副腎、骨などです。
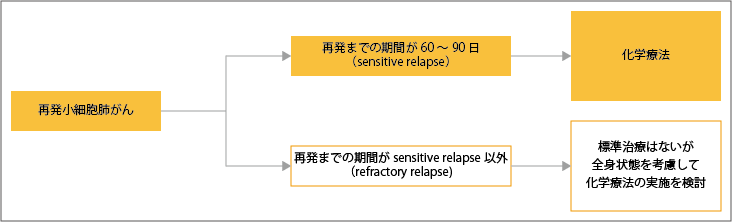
参考:日本肺癌学会. 肺癌診療ガイドライン ―悪性胸膜中皮腫・胸腺腫瘍含む― 2023年版.III.小細胞肺癌(SCLC).1再発小細胞肺癌の樹形図より作成
骨転移に対する治療
肺がんの骨転移に対する治療は、薬物療法を基本として放射線治療も併用されることがあります。骨に転移すると疼痛や骨折の危険があるため、痛みを緩和したい場合、骨折リスクが高い場合、まひなどの神経症状が予測される場合に放射線治療が行なわれます。また、痛みの緩和や骨折予防のためにビスフォスフォネート製剤やデノスマブが使われることもあります。
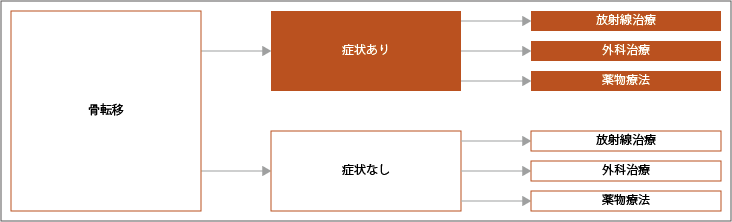
参考:日本肺癌学会. 肺癌診療ガイドライン ―悪性胸膜中皮腫・胸腺腫瘍含む― 2023年版.II.非小細胞肺癌(NSCLC).8転移など各病態に対する治療より作成
脳転移に対する治療
脳転移に対しては、放射線治療が行われます。脳全体に放射線を照射する「全脳照射」と、転移した部分をピンポイントで放射線を照射する「定位放射線治療」があります。患者さんの病状、状態、個数、大きさなど患者さん個別の状況を検討して、症状緩和を目的として行われます。
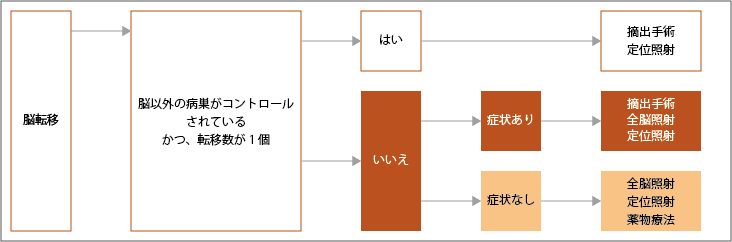
参考:日本肺癌学会. 肺癌診療ガイドライン ―悪性胸膜中皮腫・胸腺腫瘍含む― 2023年版.II.非小細胞肺癌(NSCLC).8転移など各病態に対する治療より作成
胸部病変の治療
縦隔・肺門病変による気道狭窄や上大静脈狭窄など胸部内の腫瘍増大に伴う症状がある場合は、根治治療が困難でも症状の緩和や延命を目的とした胸部への放射線治療が推奨されています。
がん性胸膜炎の治療
胸腔穿刺やドレナージによるがん性胸膜炎に対しては、胸膜癒着術が推奨されています。また、薬物療法未治療の患者さんに対しては、胸膜癒着術の代わりに細胞傷害性抗がん薬が治療選択肢として考慮されています。
がん性心膜炎の治療
心のう穿刺やドレナージによるがん性心膜炎に対しては、短期の症状緩和を目的に心膜癒着術が考慮されています。
少数転移に対する治療
転移臓器や転移戸数が限られている患者さんでは、薬物用法により病勢が安定している場合は、増悪までの期間を延長させるメリットが得られる可能性があるため局所治療(切除もしくは放射線治療)が考慮されています。
参考文献:日本肺癌学会. 肺癌診療ガイドライン ―悪性胸膜中皮腫・胸腺腫瘍含む― 2023年版.金原出版

