第4回日本がんサポーティブケア学会 「がん悪液質ハンドブック」に書けなかった重要なこと
2019.10 提供●がんサポート
がん悪液質は、簡単に言えば「がんを有するだけで、ダイエットをしているわけでもないのに、体重が落ち、筋肉が減り、足腰が弱る現象」である。進行がん、とくに肺がんや消化器がんで発症の頻度が高く、診断時に3割以上、終末期には8割以上の患者に認められる。日本がんサポーティブケア学会(JASCC)では、がん悪液質への理解を深め、臨床に役立ててもらうため「がん悪液質ハンドブック」を作成した(2019年3月,文献1)。その著者の一人で静岡県立静岡がんセンター呼吸器内科医長の内藤立暁氏(JASCC Cachexia部会)は「ハンドブックに書けなかった重要なこと」と題して報告した。その中で、同氏はがん悪液質の診断・評価、治療などに関する以下の4つの課題を挙げ、今後のガイドライン策定に向けた方向性を示した。
1.「悪液質」と「前悪液質」をどのように診断するか?
内藤氏がまず課題として指摘したのは「どう診断するか?」だ。がん悪液質の進行度は、「前悪液質」、「悪液質」、「不応性悪液質」の3ステージに分類される(図1)。
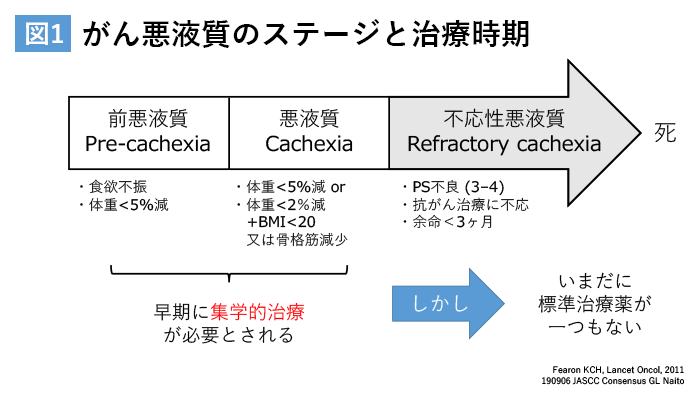
このうち真ん中の「悪液質」の診断については、以下の様な診断基準が用いられている。
① 5%を超える意図しない体重減少(過去6カ月以内)
② 2%以上の意図しない体重減少、かつBMIが20未満
③ 2%以上の意図しない体重減少、かつ骨格筋量が減少
がんを有する患者で、これら3つの条件のいずれかに合致すれば、がん悪液質と診断される(文献2)。がん悪液質の多くの患者は経口摂取不良、全身炎症を伴うことが多い。①と②は体重、身長測定と過去の体重についての簡単な問診で評価できる。しかし、③に含まれる「骨格筋量」は、二重エネルギーX線吸収測定法(DEXA)と呼ばれる特殊な測定機器を用いたり、CT画像を画像解析ソフトウェアで解析したりしなければ測定することができず、多忙な臨床現場に導入することは難しい。最近報告された、フランス、ベルギーの多施設研究によると、がん悪液質の9割は、①と②の基準のみで診断が可能であった。つまり、煩雑な骨格筋の測定をしなくても、9割の患者を診断できるという結果であった(文献3)。
一方、「前悪液質」については、定義そのものが明確ではないが、以下の様な診断基準がよく用いられる。
① 2~5%の意図しない体重減少
② 体重減少の有無に関わらず、「食欲不振」がある
③ 体重減少の有無に関わらず、骨格筋量が減少
先ほどの研究では、「前悪液質」の約6割は体重減少、食欲不振、BMIで診断され、残りの4割は、骨格筋量の測定が必要だった(文献3)。
これらのデータから内藤氏は「実地臨床では、体重減少とBMIの情報のみで大方の悪液質の患者と、6割の前悪液質の患者を判断することができる。前悪液質をより多く見つけるには、手間はかかるが骨格筋量を測るのがよいのではないか」と提案した。しかし、一方で2%程度の体重変化は、食事や飲水などによる生理変動でも生じうるわずかな変化である。従って、実地臨床では測定値のわずかな変動に振り回されることなく、「大事なのは、“できるだけ早く悪液質を見つけよう” という原則を忘れないことではないか」と強調した。
2.がんの治療中に悪液質は変化するか?
がん悪液質における特徴的な症候は体重の減少だ。主な原因は、骨格筋と脂肪組織の合成減少と分解促進であるが、これらはがん治療の効果、副作用にも影響される。がんの治療経過中の体重の推移は患者により様々である。内藤氏らが、非小細胞肺がんで初回化学療法の134例を追跡したところ、体重が減る患者もいれば、増える患者もいるなど多様であった。診断時に悪液質だった患者の割合は46%、半年後46%、1年後26%であり、時間と共に増加するというわけではなかった。そしてどの時点においても、悪液質の有無が、それ以後の生存期間の長さを左右していた(文献4)。さらに、詳しく経過を追うと、治療中に悪液質、非悪液質は入れ替わり、ステージも変わることがわかった(図2)。
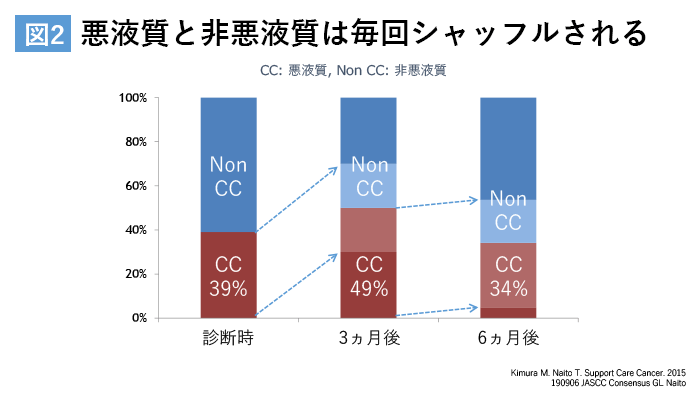
この観察から内藤氏は「がん悪液質の状態は、がん治療中に変化してゆく。がん治療の全経過にわたり、非悪液質、前悪液質に留まる継続的介入が必要ではないか」と強調した。
3.現在の治療手段は?
がん悪液質では早期からの集学的治療が必要と考えられているが、具体的な標準治療は確立されていない。しかし、何も対処ができないわけではなく、悪液質の進行を食い止めるために私たちが早期からできることもある。その1つが、摂食関連症状(NIS:nutrition impact symptoms)に対する対策である。NISは、摂食を妨げる症状を指し、がんそのものによる痛み、呼吸困難、抑うつ、化学療法による悪心・嘔気、口内炎(口腔粘膜障害)、味覚・嗅覚障害などがある。悪液質による代謝障害は現在時点では有効な治療がないため対策は難しいが、NISによる摂食量の減少は、適切な鎮痛薬、制吐療法、口腔ケア、栄養カウンセリングなど、多職種の協力によって予防対策を講じることができ、患者の体重減少を阻止できる可能性がある(図3)。
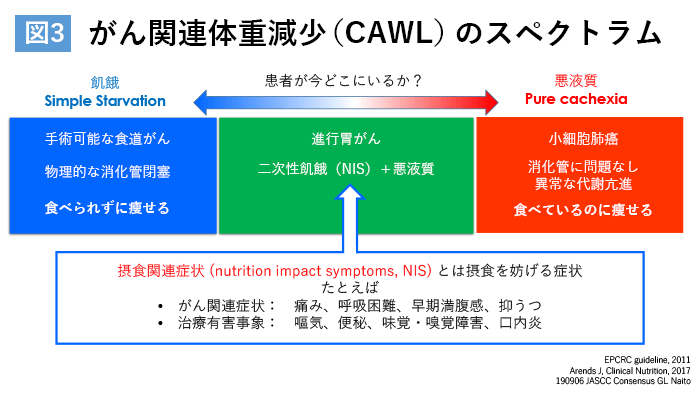
内藤氏によると、「実臨床では、悪液質による体重減少とNISによる体重減少は常に混在している。悪液質に対する有効な治療法はまだないが、NISによる二次性飢餓を軽減し、体重減少を防げば、がん治療の継続や予後の改善につながる可能性がある」という。また、NISへの対策としては、多職種チームで栄養介入していく必要があり、とりわけ栄養士の存在は欠かせないとした(図4)。
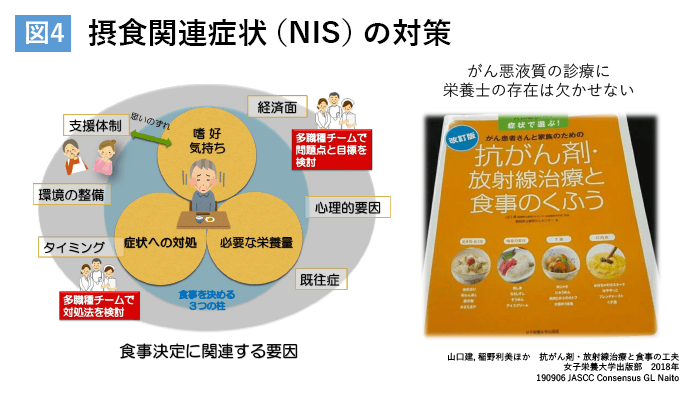
さらに、栄養療法と運動療法の併用についても触れ、「エビデンス(科学的根拠)は得られていないものの、ESPEN(欧州臨床栄養・代謝学会)のガイドライン(文献5)では、栄養療法と運動の併用を推奨しており、運動習慣の維持・促進が重要」と述べた。
4.がん悪液質の医療のゴールは?
現在までに、がん悪液質に対する複数の治療薬の開発が精力的に進められており、そのうち3剤は第Ⅲ相試験まで進んでいる(図5)。
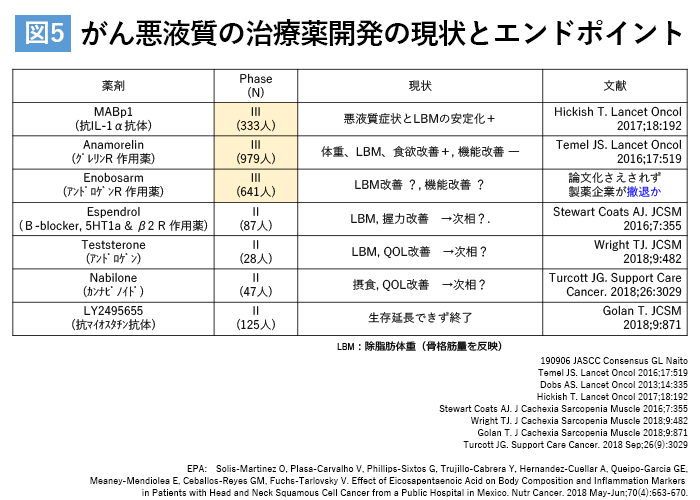
その1つがMABp1(ヒト抗IL-1α抗体)だ。インターロイキン1α(IL-1α)やそれによって誘導されるIL-6などのサイトカインは、発熱・倦怠感・食欲不振や骨格筋の減少を引き起こす。MABp1は、このIL-1αに特異的に結合し、作用を中和する。試験の対象となったのは、がん悪液質を有する切除不能・転移性大腸がん患者333例。
その結果、プラセボ群に比べ、悪液質症状の有意な改善、除脂肪体重(LBM:骨格筋量の指標)の安定が得られた。しかし、欧州医薬庁(EMA)は、①明らかなLBMとQOL(生活の質)の改善が得られていない、②緩和医療を受ける脆弱な患者には許容し難い感染リスクの増加がある、として承認申請を棄却した。また、グレリン様作用薬のアナモレリン(anamorelin)は、日本を含め世界中でいくつかの試験が行われ、食欲、体重、LBMの増加が認められた。しかしこれも、わずかなLBMの増加しかみられていない、身体機能やQOLの信頼に足る「臨床に直結する成果」を得られていない、潜在的リスク(心毒性)が利益を上回っている、などの理由から棄却されている。
さらに、エノボサーム(enobosarm)に至っては、第Ⅲ相試験は済んでいるものの、その後の報告はない。内藤氏が過去16年間に発表されたがん悪液質のランダム(無作為)化比較臨床研究で用いられた評価項目を調べたところ、最もポピュラーな評価項目は、体重、QOL、LBMの3つであったが、その他にも研究者によって様々な評価項目が用いられており、一貫していなかった(文献6)。また、そのような評価項目の「臨床的に意義のある変化」を定義している研究は極めて少なかった。さらに、薬物治療で骨格筋量を増やす効果が得られても、必ずしも身体機能やQOLが回復するとは限らないことも報告されている。
こうした点を踏まえて内藤氏は、がん悪液質の医療のゴールについて、①古典的な評価項目(体重やLBM)の改善のみを追求しても標準治療には成り得ない、②身体機能やQOLを改善することが実臨床では重要なゴールである、そして③「臨床に直結する成果」は何か、患者、研究者、規制当局が合意できる研究ならびに実臨床のゴール設定について議論を深める必要がある-と述べ報告を締めくくった。取材・文●「がんサポート」編集部
文献)
1. 日本がんサポーティブケア学会. がん悪液質ハンドブック. 2019年3月
2. Fearon K et.al., Definition and classification of cancer cachexia: an international consensus. Lancet Oncol. 2011 May;12(5):489-95.
3. Antoun S et.al., Staging of nutrition disorders in non-small-cell lung cancer patients: utility of skeletal muscle mass assessment. J Cachexia Sarcopenia Muscle. 2019 Aug;10(4):782-793.
4. Kimura M et.al., Prognostic impact of cancer cachexia in patients with advanced non-small cell lung cancer. Support Care Cancer. 2015 Jun;23(6):1699-708.
5. Arends J et.al., ESPEN guidelines on nutrition in cancer patients. Clin Nutr. 2017 Feb;36(1):11-48.
6. Naito T. Evaluation of the True Endpoint of Clinical Trials for Cancer Cachexia. Asia Pac J Oncol Nurs. 2019 Jul-Sep;6(3):227-233.
がんと栄養相談窓口
がん患者さん、そのご家族のためのがんと栄養の相談窓口です。気軽にご相談ください。
- どんなレシピがあるのか知りたい
- 必要な栄養って何?
- カロリーはどのくらい?・・・など


