早期胃がん、外科的手術をせずに根治可能な治療 内視鏡的治療EMR/ESDの方法と適応

2018.3 取材・文:町口充
胃がんの治療に関する最新情報は、「胃がんを知る」をご参照ください。
胃がんは、胃壁が食物と接する一番内側の粘膜内にでき、次第に増殖して壁の深部へと広がっていきます。粘膜内に留まっている早期のがんであればリンパ節やほかの臓器への転移がほとんどないため、開腹しなくても内視鏡的治療で完全に切除し、根治させることも可能です。また、内視鏡的切除の技術の普及や治療実績が積み重ねられるなかで適応範囲も拡大しており、早期の段階で胃がんが見つかれば「お腹を切らずに治す」時代になっています。
早期胃がんに対する低侵襲の内視鏡的治療 EMRとESDとは
胃がんの根治を目指す一番の治療法はがんを切除して完全に取りきることです。それには外科的手術によって切除するしかないと思われがちですが、もう1つの方法として内視鏡的切除があります。先端にCCDと呼ばれる半導体素子(超小型カメラ)を備えた電子スコープを口から胃の中に挿入し、中の様子を直接観察するとともに治療器具を使ってがんを切除するのが、内視鏡的切除です。
外科的手術の場合、開腹手術はお腹の切開傷が大きいため術後の回復に時間がかかるうえ、臓器の一部を取り去るため後遺症を伴います。出血や感染、縫合不全などの合併症の心配もあります。腹腔鏡下手術にしても、お腹の傷が小さくてすむメリットはあるものの胃の一部を切除する点では開腹手術と同じであり、手術による合併症のリスクはあります。
これに対して、お腹を全く傷つけずに胃の内側からがんだけを切除するのが内視鏡的治療です。開腹手術に比べて治療による侵襲が格段に低く入院期間も短くてすみ、治療後のQOL(生活の質)を損なわないなどの利点があります。
ただし、内視鏡的切除の適応となるのは、リンパ節転移を認めない、がんが粘膜内に留まっている早期の胃がんです。リンパ節は胃の外部にあるので、内視鏡的治療では切除できないため、リンパ節転移やその可能性のあるがんは、適応になりません。
胃がんの内視鏡的治療には、おもに内視鏡的粘膜切除術(EMR)と内視鏡的粘膜下層剥離術(ESD)の2種類があります。
EMRは、生理食塩水などの液体を病巣の下の粘膜下層に注入して病変部を浮き上がらせ、内視鏡の先端から伸びるスネアと呼ばれる輪状のワイヤーで浮き上がった部分を締め上げ、高周波電流を流して焼き切り、回収する方法です(図1)。
ただし、この方法ではスネアの大きさの点から、1回に切り取れる範囲が限られているため、大きい病変の場合は1回で切除しきれず、何回かに分けて分割して切除するしかありません。ところが、分割して切除すると再発率が高くなるという問題があります。
EMRの弱点を克服する方法として登場したのがESDです。病変の下の粘膜下層に液体を注入して病変部分を浮き上がらせるまではESDと同じです。そのあとは、スネアではなく電気メスであらかじめマーキングした部分の全周を浅く切っていきます(図2)。次に専用のナイフを使い、病変部分とその下の粘膜下層を高周波電流で焼きながら剥離させて切り離し回収します。最終的に病変を確実に含んだ一回り大きな粘膜を一括で切除します。
この方法では、粘膜内に留まっているがんならどんな大きさでも1回の治療で取りきることができ、しかも取り残しが少ないという利点もあります。胃がんの内視鏡的切除は、かつてEMRが主体でしたが、今では主としてESDが行われています。
図1:EMR(内視鏡的粘膜切除術)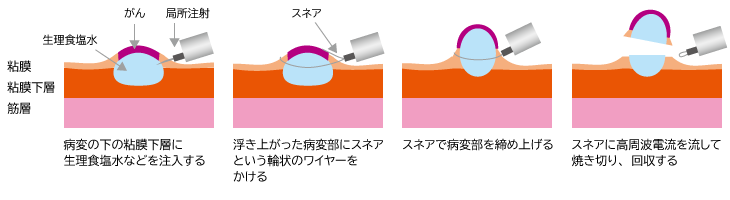
図2:ESD(内視鏡的粘膜下層剥離術)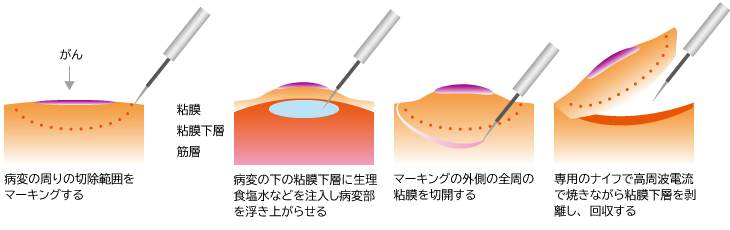
最新版、胃癌治療ガイドライン第5版で、対象外だった病変にも適応拡大されたESD治療
早期胃がんに対するESD治療が保険適用となったのは2006年です。その後、10年あまりの間に技術のさらなる進歩とともに症例数が増えていくなかで、従来は対象外とされた病変についても臨床試験のエビデンスを得て適応が拡大しています。
内視鏡的切除の適応になるかどうかは、治療前の内視鏡検査で判断されます。具体的には、がんが胃壁の表面に広がる大きさ、胃壁内へ広がる深さ(深達度)を調べて、組織の内側の一番浅い粘膜内に留まっているがんかどうか、分化型か悪性度の高いとされる未分化型か、病変部分に潰瘍を伴っているかどうかによって、総合的に判断されます。
2018年1月に改訂された最新の胃癌治療ガイドライン第5版では、特にESDについて、適応対象が拡大されました(表1)。これによると、十分なエビデンス(臨床試験の結果などで得られた科学的根拠)があり日常診療としてEMRあるいはESDによる治療を推奨できる「絶対適応病変」として、「2cm以下の粘膜内がんで、分化型のがんであり、病変部分に潰瘍を伴っていないと判断される病変」があげられています。
EMRは2cmを超えるものは一括切除ができませんが、ESDは、がんの大きさにかかわらず一括切除が可能です。そのため、同ガイドラインでは、ESDのほうについては、「絶対適応病変」の適応範囲をさらに広げて、2cmを超えていても分化型で潰瘍を伴わない粘膜内がんを適応としました。つまり、ESDでは、粘膜内に留まっている分化型で潰瘍を伴わないがんであれば、治療に時間はかかるものの10cm以上のがんでも切除が可能となったのです。
このほか、潰瘍を伴っているがんでも、3cm以下の分化型の粘膜内がんであれば、ESDによる切除は「絶対適応病変」として推奨されています。
表1:EMR・ESDの適応
| 適応 | 深達度 | 大きさ | 悪性度 | 潰瘍 | |
|---|---|---|---|---|---|
| EMR・ESD | 粘膜内に留まっている(cT1a) | 2cm以下 | 分化型 | なし | 絶対適応病変 |
| ESD | 粘膜内に留まっている(cT1a) | 2cm以上 | 分化型 | なし | 絶対適応病変 |
| ESD | 粘膜内に留まっている(cT1a) | 3cm以下 | 分化型 | あり | 絶対適応病変 |
| ESD※ | 粘膜内に留まっている(cT1a9 | 2cm以下 | 未分化型 | なし | 適応拡大病変 |
※現時点では、長期予後に関するエビデンスが乏しく絶対適応としない
適応範囲をわずかに超えたがんでは条件つきでESDが可能
未分化型のがんは悪性度が高くリンパ節転移のリスクがあるため、基本的には内視鏡的切除の適応外とされています。ただし、未分化型であっても2cm以下の粘膜内がんで潰瘍は伴っていないものについて、今回の改訂では、ESDを慎重に試みてよいとして「適応拡大病変」と位置づけられています。現時点では、長期予後に関する十分なエビデンスが示されていないため「絶対適応」とはせず、現在実施中の臨床試験の結果が出るまでは臨床研究として行われます。
もう1つ、内視鏡的切除の適応には「相対適応病変」が設けられました。例えば、がんが粘膜を超えて胃の壁の深くまで達していたり、未分化型や潰瘍を伴う大きな病変だった場合は、リンパ節転移のリスクが高いため内視鏡的切除の適応にならず、本来なら選択されるのは開腹手術による胃切除です。ただし、何らかの理由で外科的手術による胃切除を選択しがたい早期胃がんに対して、内視鏡的切除の施行を認めるのが、この「相対適応病変」です。
例えば、がんがごく浅い粘膜下層に入り込んでいる場合や、粘膜内に留まる分化型でも潰瘍があるがんで3.5cmの大きさがある場合など、内視鏡的切除の適応外とはいってもごく小さな超過である場合です。このような場合は、リンパ節転移のリスクもそれほど高いとはされません。加えて、そもそもESDによる治療は、粘膜下層を剥離し切除するので、粘膜下層まで及ぶがんも、技術としては切除が可能です。
具体的な例でいうと、患者さんが80代、90代の高齢者の場合や、がん以外のほかの病気が併存していた場合、手術による合併症のリスクのほうが高くなることもあります。このような理由によって、外科的手術よりも内視鏡的切除を患者さんが希望するとき、リンパ節転移の危険性があることを考慮しつつ、患者さんの理解と同意をもとに、「相対適応病変」として内視鏡的切除が選択されることもあります。
病理検査で根治性が確認されれば、追加治療は必要なし
内視鏡的治療では、鎮静薬と鎮痛薬を使うので、眠っている間に痛みを感じることはなく治療が終わります。治療時間は3cmぐらいなら1時間ほどで終わりますが、大きいと数時間かかることもあります。病変部分の剥離や切除によって大きな潰瘍ができたり、出血する場合があるため、数日間は入院して術後の管理が必要になります。当院では、木曜日に治療を行って月曜日に退院するというスケジュールをとっています。
内視鏡治療の合併症として代表的なものは出血です。もともと粘膜下層には毛細血管が豊富なためで、高周波ナイフで剥離すると出血が生じます。ほとんどの出血は治療中に凝固止血するので問題はありません。また、剥離したあとの粘膜は再生して元に戻るため、後遺症を残すこともありません。ただし、まれではありますが、治療後に出血することがあります。この場合は内視鏡を用いて止血します。また、胃の壁は非常に薄いので治療中に胃の壁に穴があく(穿孔)ことがあります。これもきわめてまれですが、穿孔はすぐにわかるので、その場で内視鏡的にクリップで閉鎖します。
治療の後は、切除によって根治が得られたかどうかを検査によって確かめます。事前の内視鏡検査では、がんの表面的な広がりは確かめられても、がんの深さ(深達度)を正確に知ることが難しいため、切り取ったがん細胞を病理検査で詳しく調べます。この検査で重要なのは、がんが完全に取りきれたか、リンパ節転移の可能性があるかどうかの2つの要素です。
その結果、2つの要素を十分にクリアし、根治が得られたと判断されれば治療は成功です。追加の治療は必要なく、その後は年に1~2回程度、内視鏡検査、腹部超音波検査、CT検査で経過観察をします。
また、検査の段階では内視鏡治療適応病変と判定されていても、切除後の病理検査によってがんが内視鏡的治療の適応外だったと判定されることがあります。そのような場合には、追加の治療として外科的手術を行い、病変の再切除とリンパ節郭清をすることが必要となります。そのような場合でも、早期の胃がんであれば、95%以上の割合で根治が可能です。
今後は、リンパ節転移の疑いがある症例に対してもESDが活躍するようになるかもしれません。現在、当院を含めた一部の施設では、リンパ節への転移があるかどうかを調べるため、先進医療として胃がんにおける腹腔鏡下センチネルリンパ節生検を行っています。センチネルとは「見張り番」の意味で、がんが最初に転移するリンパ節です。そのため、センチネルリンパ節に転移がなければ、その先のリンパ節への転移の可能性がないと判断します。
プロフィール
川久保博文(かわくぼ・ひろふみ)
1999年 慶應義塾大学医学部一般・消化器外科助手
2013年 慶應義塾大学医学部一般・消化器外科専任講師
2017年 慶應義塾大学医学部一般・消化器外科准教授

